- 285.50 KB
- 2022-04-29 14:28:21 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'2018年宁夏回族自治区公立医院药品补充直接挂网采购文件采购编号:NYC/YP201802宁夏药品采购中心二○一八年五月31
目录第一部分采购活动安排………………………………………………………2第二部分药品采购须知……………………………….……………………3第三部分单元划分规则……………………………….……………………10第四部分药品挂网采购目录.………………………………………………20第五部分申报文件参考格式……………………………….………………2221
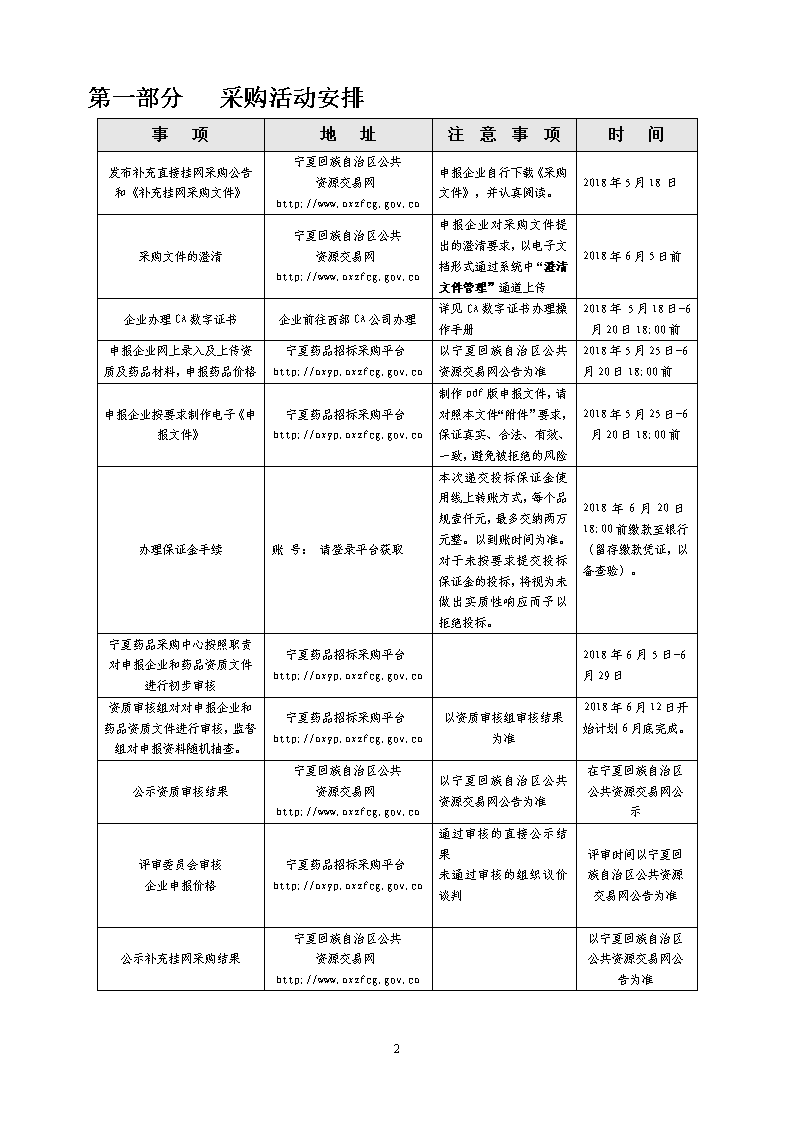
第一部分采购活动安排事项地址注意事项时间发布补充直接挂网采购公告和《补充挂网采购文件》宁夏回族自治区公共资源交易网http://www.nxzfcg.gov.cn申报企业自行下载《采购文件》,并认真阅读。2018年5月18日采购文件的澄清宁夏回族自治区公共资源交易网http://www.nxzfcg.gov.cn申报企业对采购文件提出的澄清要求,以电子文档形式通过系统中“澄清文件管理”通道上传2018年6月5日前企业办理CA数字证书企业前往西部CA公司办理详见CA数字证书办理操作手册2018年5月18日-6月20日18:00前申报企业网上录入及上传资质及药品材料,申报药品价格宁夏药品招标采购平台http://nxyp.nxzfcg.gov.cn以宁夏回族自治区公共资源交易网公告为准2018年5月25日-6月20日18:00前申报企业按要求制作电子《申报文件》宁夏药品招标采购平台http://nxyp.nxzfcg.gov.cn制作pdf版申报文件,请对照本文件“附件”要求,保证真实、合法、有效、一致,避免被拒绝的风险2018年5月25日-6月20日18:00前办理保证金手续账号:请登录平台获取本次递交投标保证金使用线上转账方式,每个品规壹仟元,最多交纳两万元整。以到账时间为准。对于未按要求提交投标保证金的投标,将视为未做出实质性响应而予以拒绝投标。2018年6月20日18:00前缴款至银行(留存缴款凭证,以备查验)。宁夏药品采购中心按照职责对申报企业和药品资质文件进行初步审核宁夏药品招标采购平台http://nxyp.nxzfcg.gov.cn2018年6月5日-6月29日资质审核组对对申报企业和药品资质文件进行审核,监督组对申报资料随机抽查。宁夏药品招标采购平台http://nxyp.nxzfcg.gov.cn以资质审核组审核结果为准2018年6月12日开始计划6月底完成。公示资质审核结果宁夏回族自治区公共资源交易网http://www.nxzfcg.gov.cn以宁夏回族自治区公共资源交易网公告为准在宁夏回族自治区公共资源交易网公示评审委员会审核企业申报价格宁夏药品招标采购平台http://nxyp.nxzfcg.gov.cn通过审核的直接公示结果未通过审核的组织议价谈判评审时间以宁夏回族自治区公共资源交易网公告为准公示补充挂网采购结果宁夏回族自治区公共资源交易网http://www.nxzfcg.gov.cn以宁夏回族自治区公共资源交易网公告为准21
保证金的退还保证金采用网络退还的方式,请关注宁夏回族自治区公共资源交易网http://www.nxzfcg.gov.cn1.未中标人的保证金,在定标结束后无息退还。2.中标人的保证金,在挂网结果公示后无息退还。以宁夏回族自治区公共资源交易网公告为准申报企业应注意:如上述事项所安排的事件及通知内容发生变动,以http://www.nxzfcg.gov.cn(宁夏回族自治区公共资源交易网)和http://nxyp.nxzfcg.gov.cn(宁夏药品招标采购平台)上发布的通知为准,请申报企业及时关注网上发布的最新信息。第二部分药品采购须知一、总则1、原则(1)坚持公开、公平、公正,必须做到程序合法有效,招标采购的信息、过程和结果公开,接受社会监督;(2)坚持以省为单位的药品集中采购原则;(3)坚持公开透明、分类采购、量价挂钩、全程监督的药品集中采购原则;(4)坚持政府引导、市场主导、充分竞争、优胜劣汰的药品配送原则;(5)坚持网上采购、上下联动、集中支付、动态管理的药品供应保障监督管理原则。2、公告方式药品集中采购公告通过公开的报刊媒体和本次招标信息平台—宁夏回族自治区公共资源交易网(http://www.nxzfcg.gov.cn)的宁夏药品招标采购平台发布。3、采购方式直接挂网采购。直接挂网采购药品评审不划分竞价组,不进行经济技术标评分,不设置挂网入围数量限制。4、采购目录(1)《2016年宁夏回族自治区公立医院直接挂网采购药品目录》;(包括《2015年宁夏回族自治区公立医院药品招标采购目录》中流标的药品品规);(未取得宁夏回族自治区公立医院药品集中采购直接挂网资格的药品品规,均可依规参加本次宁夏回族自治区公立医院药品补充直接挂网采购活动。)(2)《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》中未纳入《2015年宁夏回族自治区公立医院药品招标采购目录》和《2016年宁夏回族自治区公立医院直接挂网采购药品目录》的药品品规,具体到药品通用名、剂型和规格;21
(未取得宁夏回族自治区公立医院药品集中采购直接挂网资格的药品品规,均可依规参加本次宁夏回族自治区公立医院药品补充直接挂网采购活动。)(3)收录在《中国上市药品目录集》中的药品生产企业及其药品品规,但未取得宁夏公立医院药品集中采购中标(挂网、成交)资格的药品生产企业及其药品品规(时间截止为2018年5月17日18时)以及未收录在《中国上市药品目录集》中通过质量和疗效一致性评价的药品(2018年5月17日前,国家药监总局公布的通过质量和疗效一致性评价的药品,以国家药监总局公告为准)和视同通过质量和疗效一致性评价的药品(2016年3月4日-2018年5月17日,国家药监总局按新化学药品注册分类批准上市的仿制药,以国家药监总局的药品批件为准)。(未取得宁夏回族自治区公立医院药品集中采购直接挂网资格的药品品规,均可依规参加本次宁夏回族自治区公立医院药品补充直接挂网采购活动。)5、采购周期从药品集中采购挂网结果正式公布起,采购周期原则上不少于12月。如挂网药品采购周期需要变更或调整,则以自治区药招办文件为准。6、实施范围全区县级(含)以上人民政府、国有企业(含国有控股企业)等举办的非营利性医疗机构(含村卫生室)必须参加医疗机构药品集中采购工作。鼓励其他医疗机构自愿参与。7、适用范围参加药品集中采购活动的招标人、医疗机构、药品挂网企业、药品配送企业、招标机构及其它各方当事人,适用本须知。8、组织机构(1)药品集中采购工作组织领导机构。宁夏回族自治区医疗机构药品器械统一招标采购领导小组(以下简称“自治区药招领导小组”)负责全区药品集中采购工作。承担制定全区医疗机构药品集中采购工作政策,研究药品集中采购工作的重大问题,协调各部门按照职责分工做好药品集中采购工作。宁夏回族自治区医疗机构药品器械统一招标采购领导小组办公室(以下简称“自治区药招办”)负责组织实施药品集中采购工作。成立评审委员会,负责药品集中采购评审工作;成立评审监督委员会,负责药品集中采购评审全过程监督。自治区药招领导小组各成员单位根据工作职责分工,加强药品集中采购工作的协调配合和监督管理。(2)药品集中采购工作机构。自治区公共资源交易管理局(宁夏药品采购中心)负责药品集中采购工作具体执行。承担搭建非盈利药品集中采购服务平台,提供服务,维护管理平台,开展业务咨询,接收相关申(投)诉。二、报名及材料申报21
本次宁夏回族自治区公立医院药品补充直接挂网项目相关资质维护采用网上维护方式,申报材料上传至宁夏药品招标平台加盖电子签章后方可生效。1、以下情况的企业不具有申报资格:(1)2016年以来,药品生产企业申报药品有劣药记录或被国家食品药品监督管理总局指明特定企业生产的药品召回或停止使用的,非申报药品有2次(含)以上劣药记录或有生产假药记录。(2)2016年以来,企业有行贿行为被检察机关调查处理。(3)同一药品企业的所有申报药品只可授权委托1个被授权人,2个(含)以上被授权人申报的。(4)食品药品监督管理部门勒令停产或停业整顿的企业及其药品,在本次挂网报名截止日期前,仍在停产或停业整顿期间内未恢复生产的。(5)企业申报药品代理权等存在争议,且在企业报名截止日前争议仍未解决的,不接受该企业申报材料和报名。(6)在我区药品供应保障工作中,因严重违规给予2年内不能参加宁夏药品集中采购活动处理的生产企业,报名截止日期仍然在处理期内。(8)未缴纳保证金的。(9)法律法规规定的其他条件。2、资质证明文件Ⅰ.药品生产企业册(1)企业资质文件封面(详见参考格式7)。(2)申报函(包括申报函附件,详见参考格式1)。(3)法定代表人授权书[进口药品全国代理需提交代理协议书或由境外企业出具的总代理证明]。(详见参考格式3、4)(4)企业基本情况。(详见参考格式2)(5)申报药品基本信息表(详见参考格式5)。(6)药品生产企业提供:《药品生产许可证》和《药品GMP认证证书》;药品生产企业设立的仅销售本公司药品的商业公司、进口药品国内总代理(含一级代理)提供《药品经营许可证》《药品GSP证书》。(7)《企业法人营业执照》;(8)药品生产企业保证按时足量供货承诺函(详见参考格式6)和执行药品采购“两票制”承诺函(企业自拟);(8)2016年以来,药品生产企业两年以来无生产(或无经营)假(劣)药品承诺函;(9)2016年以来,药品生产企业注册所在县级以上检察机关出具的药品生产企业两年以来无单位行贿犯罪记录书面证明。21
Ⅱ.药品册(1)药品资质证明文件封面(详见参考格式8)。(2)《药品注册批件》(国产药品提供)、《进口药品注册证》(进口药品提供)或《医药产品注册证》(港澳台地区药品提供)。(3)药品说明书和包装盒;(4)申报产品2016年以来市级(含)以上药品检验机构出具的全检报告。进口药品、港澳台地区药品提供国家食品药品监督管理总局授权口岸药品检验机构出具的《进口药品检验报告书》。注:企业除按上述要求填报、上传企业药品信息,资质证明文件外,还需按上述企业册和药品册要求制作《电子申报文件》并上传。格式要求:PDF版,100M以内。3、材料申报说明(1)生产企业提交的所有文件材料及往来函电均使用中文,外文资料必须提供相应的中文翻译文本,且需经过市级以上公证处公证。(2)同一生产企业有多个申报药品的,其药品册材料,应以申报药品为单位,将每个药品的相关材料汇集,按照拟申报药品汇总表的填写顺序制作电子文档。(3)所有申报材料必须清晰完整方可上传,否则按无效文件处理;(4)申报企业准备材料时应注意:所有证照期限应在有效期内;同一药品的所有材料上的生产企业名称是否一致,如不一致,应递交相关行政部门出具变更批准文件和相关的证明;(5)申报企业填报剂型等相关资料时,要严格按照《采购文件》规定填报,如出现误差,由申报企业自负;(6)本次挂网采购原则上不提交样品,但采购人保留因招标等相关事宜需要随时要求申报企业提交样品的权利。4、采购文件的响应和澄清(1)响应:申报企业应认真阅读采购文件中所有的事项、格式、条款和规范等要求。如果申报企业没有按照采购文件的要求上传全部资料,或者申报文件没有对采购文件做出实质性响应,由此造成的后果由申报企业负责。(2)澄清:申报企业对采购文件提出的澄清要求,应在挂网截止时间前五日内,以电子文档形式通过系统中“澄清文件管理”通道上传,招标机构对申报企业的书面澄清,将以公告形式通过宁夏公共资源交易网(http://www.nxzfcg.gov.cn)的“药品采购”公告栏予以答复。澄清系统需用CA数字证书登陆后方可使用。注:有关澄清问题申报企业可登陆宁夏公共资源交易网药品采购公告栏进行查询。申报企业有义务登陆查看相关信息,否则由此造成的不良后果由申报企业自负。没有在本次招标信息平台上发布的任何答复均不作为申报企业制作申报文件的依据。5、申报文件的澄清(121
)采购人对申报文件中含义不明确的内容可要求申报企业作必要的澄清或者说明。有关澄清的答复可以书面形式提交。但澄清或者说明不得超出采购文件的范围或者改变采购文件的实质性内容。(2)如需要澄清的问题较多,采购人可召开会议邀请申报企业到会予以澄清。6、投标企业网上信息录入说明:(1)申报企业首先办理CA数字证书(详见“CA数字证书办理指南”),企业使用CA数字证书登录“宁夏药品招标采购平台”(http://nxyp.nxzfcg.gov.cn),进行企业信息录入和相关申报药品信息录入,上传企业和药品资质证明文件,按要求格式上传电子申报文件(PDF版)。(2)申报信息证明文件的录入及上传①申报企业须在规定时间内按要求及时录入企业及药品相关信息,上传企业和药品资质证明文件以及《电子申报文件》,申报企业必须保证报送的企业信息及药品信息的真实性、准确性并承担相应的法律责任。②如申报企业未在规定时间内提供《电子申报文件》或相关补充文件,招标人可认定该申报企业自行放弃申报资格,由此而产生的一切后果由申报企业自负。四、申报文件的审核1、资质审核组负责审核生产企业和申报产品的资质材料。自治区公共资源交易管理局负责组织评审委员会审核企业申报价格。评审委员会根据产品预判价审核企业申报价格,通过审核的,予以公示、公布。未通过审核的,由自治区公共资源交易管理局负责组织医药专家组成议价谈判组,议价谈判组根据药品预判价与药品生产企业进行议价谈判,议定价格的,予以公示、公布。未议定价格的,不得予以直接挂网采购。2、申报企业的有效资质证明文件,均以政府相关部门的正式文件为准,政府相关网站发布的信息作为参考,若信息存在差异,需提供有关原件进行核对。3、申报企业提供的资料必须真实合法,并承担相应的法律责任。申报文件审核通过后,将成为评标的重要依据。出现提交虚假伪造资料的企业,自治区药招办有权取消其资格,2年内不得参加宁夏药品集中采购活动,并按相关规定处理。五、价格申报1、价格申报参加本次宁夏回族自治区公立医院药品补充直接挂网采购活动的药品生产企业,根据药品合理的市场价格自主申报药品价格。21
2、报价规则①报价包含配送费用及其他所有税费在内的,实际供应到医疗机构的价格。②报价需按宁夏回族自治区药品招标采购平台报价系统显示的每个产品的最小制剂单位进行报价。如显示的单位为片、粒、支、袋、枚、瓶、贴等,则以每片、每粒、每支、每袋、每枚、每瓶、每贴等进行报价,以此类推。③报价单位统一按人民币(元)报价,报价必须与对应的规格、包装单位相匹配,保留到小数点后4位。④带有附加装置的药品,报价为含附加装置的价格,附加装置不另行加价。⑤无论医疗机构的采购批量、配送费用存在何种差别,每种药品只允许有一个报价。六、评审1、评审委员会(1)在自治区卫生计生委纪检或自治区药招办工作人员的监督下,从自治区药品采购专家库中随机抽取组成评审委员会。评审委员会由参与药品采购的医疗机构15名专家组成(药学和医学专家原则上按照3:2的比例确定)。(2)评审专家与申报企业有利害关系的不能进入评审委员会,已经进入的将予以更换。(3)评审委员会应客观公正地履行职责,遵守职业道德,对所提出的评标意见承担个人责任。评审专家不得私下接触申报企业,不得收受申报企业的财物或者其他好处。评审委员会不得透露对采购文件的评标情况及评标、竞价相关情况。(4)评审委员会只对符合采购文件要求的申报品种进行评标和比较。(5)评审专家汇总审核结果并签署意见,形成专家集体评标书面意见。(6)从抽取评审专家到开始评标的时间一般不超过24小时,在抽取评审专家时,将抽取足够数量的替补专家。(7)评审专家名单在评审工作结束前必须严格保密。评审委员会完成评审后,招标机构应将所有挂网品种当场打印并编制书面报告,所有评审专家在书面报告上签字确认。2、价格评审申报企业自主报价,评审委员会根据产品预判价(综合考虑产品质量和价格认可程度,以及历史成交价格)审核企业申报价格,通过审核的,予以公示、公布。未通过审核的,由自治区公共资源交易管理局负责组织医药专家组成议价谈判组,议价谈判组根据药品预判价与药品生产企业进行议价谈判,议定价格的,予以公示、公布。未议定价格的,不予公布。3、议价谈判议价谈判专家根据药品预判价(综合考虑产品质量和价格认可程度,以及历史成交价格)与药品生产企业进行议价谈判,与生产企业议定申报药品拟挂网采购价格。21
4、挂网结果的公示与公布招标机构将在“宁夏回族自治区公共资源交易网”上公示、公布挂网结果。内容包括品种、剂型、规格、企业名称、价格等。申报企业如有异议,必须在公示期内持法人授权委托书和本人身份证向招标机构递交书面申(投)诉材料。21
单元划分规则一、2018年宁夏回族自治区公立医院药品补充直接挂网采购目录单元划分规则。单元划分原则为:同一品种、同一剂型、同一规格的药品为同一招标单元。药品分类中涉及的通用名称、剂型、规格、包装材质等有关属性,以生产批件(注册证)、质量标准、说明书及现行版药典等载明的事项为依据。《国家基本药物目录(2012年版)》列出的具体品种、剂型、规格不再进行合并。1、按品种划分(1)化学药品和生物药品为中文通用名称中表达化学成分的部分。不同盐基、酸根、溶媒、酯类衍生物、亚型、结晶水、螯合物、旋光性等归同一品种。(2)中成药的通用名为药品中文通用名称中不包含剂型的部分。2、按剂型划分(1)片剂①普通片:包括素片、糖衣片、薄膜衣片、包衣片、干压包芯片、双层片、异型片、划痕片、浸膏片等归同一单元。②含片、口腔粘附片、口颊片、舌下片、咀嚼片、润喉片、口腔崩解片归同一单元。③分散片:包括分散片、口服泡腾片归同一单元。④肠溶片:包括肠溶片、肠溶薄膜衣片归同一单元。⑤缓(控)释片:包括缓(控)释片、缓(控)释包衣片、肠溶缓(控)释片归同一单元。(2)胶囊剂①硬胶囊。②软胶囊(胶丸)。③肠溶胶囊(胶丸):包括肠溶胶囊、肠溶软胶囊等归同一单元。④微丸胶囊:包括微丸胶囊、肠溶微丸胶囊、肠溶微颗粒胶囊归同一单元。⑤缓(控)释胶囊:包括缓(控)释胶囊、肠溶缓(控)释胶囊、双释胶囊、缓(控)释微丸胶囊归同一单元。(3)颗粒剂①颗粒剂:包括颗粒剂、干糖浆颗粒剂、干混悬颗粒剂、冲剂、茶剂、茶饼剂、混悬颗粒剂、细粒剂、泡腾颗粒剂、泡剂归同一单元。②肠溶颗粒(剂)。③缓(控)释颗粒(剂):包括缓(控)释颗粒、缓(控)释干混悬剂归同一单元。备注:有糖型颗粒剂和无糖型颗粒剂应区分归不同单元(指蔗糖)。(4)散剂21
散剂、粉剂、药粉、撒布剂、撒粉、口服溶液用粉、干粉剂、冻干粉剂归同一单元。备注:按口服与外用分别归不同单元。(5)煎膏剂浸膏剂、流浸膏剂、煎膏剂归同一单元。(6)口服液体剂①口服溶液剂、口服液剂、合剂、糖浆剂、酊剂、酒剂、露剂、酏剂、膏剂、胶剂、胶浆剂、胶浆溶液、滴剂归同一单元。②口服混悬液(剂)、乳剂(液)、凝胶剂、混悬滴(剂)、胶体溶液、悬胶剂、干混悬剂归同一单元。③脂质体口服液、口服脂微乳、口服脂微球归同一单元。④缓(控)释混悬剂(液):包括缓释混悬剂(液)、控释混悬剂(液)归同一单元。备注:含糖(指蔗糖)和不含糖应区分归不同单元,既可口服又可外用归口服。(7)外用液体剂搽剂、涂剂、涂膜剂、涂布剂、外用锭剂、洗剂、冲洗剂、外用酒剂、外用酊剂、油剂、甘油剂、醑剂、漱口剂、含漱剂、灌肠剂、泡沫剂、外用胶浆剂、外用乳剂归同一单元。(8)丸剂①普通丸剂、水丸、蜜丸、小蜜丸、水蜜丸、糊丸、糖丸、糖衣丸、口服锭剂归同一单元。②大蜜丸、蜡丸归同一单元。③浓缩水蜜丸、浓缩水丸、浓缩蜜丸、浓缩糖丸归同一单元。④滴丸剂:包括滴丸、微丸。⑤缓(控)释丸:包括缓释丸、控释丸归同一单元。(9)注射剂①普通注射液。②普通粉针剂、冻干粉针剂、溶媒结晶粉针剂归同一单元。③脂质体注射液、脂微球注射液、脂微乳注射液、注射用乳剂、注射用混悬剂归同一单元。(10)软膏剂①软膏剂、乳膏剂、霜剂、油膏剂、糊剂、乳胶剂归同一单元。②外用凝胶剂。(11)贴剂①贴膏剂、贴剂、贴片、橡胶膏剂、橡皮膏剂、巴布膏剂、膏药剂、硬膏剂、亲水硬膏剂、外用敷剂、膜剂、透皮贴剂归同一单元。②缓(控)释贴片:包括控释(透皮)贴片、缓释(透皮)贴片归同一单元。(12)栓剂阴道栓、直肠栓、尿道栓、耳栓归不同单元。21
(13)植入剂植入剂、缓释植入剂归同一单元。(14)膜剂膜剂、牙周缓释膜、涂膜剂、贴膜剂归同一单元。(15)滴剂①滴鼻剂(含玻璃酸钠与不含玻璃酸钠的归不同单元)。②眼膏剂(含玻璃酸钠与不含玻璃酸钠的归不同单元)、眼用凝胶剂归同一单元。③滴耳剂。④滴眼剂(含玻璃酸钠与不含玻璃酸钠的归不同单元)。(16)气雾剂①气雾剂、粉雾剂、雾化溶液剂、吸入溶液剂、液体吸入剂归同一单元。②喷雾剂。备注:吸入与非吸入制剂应区分归不同单元。(17)阴道用制剂阴道片、阴道泡腾片、阴道胶囊、阴道软胶囊、外用阴道膜、阴道软膏剂、阴道栓归同一单元。(18)其他剂型胶剂、海绵剂、湿巾、锭剂、炙剂、熏蒸剂、点刺剂、热敷剂、曲剂、蜡棒、熨剂等归不同单元。3、按规格划分(1)同一药品剂型、规格相同的,归同一单元;同一药品剂型相同、规格不同的,原则上归不同单元;规格相同,含量不同的,原则上归不同单元。(2)造影剂含药量相同,浓度不同归不同单元。(3)脂肪乳含药量相同,浓度不同归不同单元。(4)肠内营养乳规格相同,热卡含量不同归不同单元。(5)氨基酸注射液按氨基酸组分不同归不同单元。(6)预混胰岛素混合比例不同的归不同单元。(7)注射液按装量,大容量注射液和小容量注射液归不同单元,大于或等于50ml的为大容量注射液,小于50ml的为小容量注射液。同为大容量注射液或小容量注射液,主药及其含量相同、浓度不同的,归同一单元(基础大输液除外)。(8)抗微生物药物和酶抑制剂混合制成的制剂,其中抗微生物药物及其含量相同的,原则上归同一单元。但临床使用存在较大差异的,经专家论证同意后,可归不同单元。(9)中成药口服、外用液体制剂按容量不同归不同单元(容量相同的浓缩型和普通型归不同单元);对仅以重量表示规格的中成药片剂和胶囊剂,日用量相同的归同一单元;颗粒剂等剂型主药及其含量相同,重量不同的归同一单元。21
4、其他划分(1)长链、中长链脂肪乳归不同单元。(2)不同亚型品种按药理效应、临床用途不同归不同单元。例如:干扰素α-1a、α-2a、α-1b、α-2b等不同亚型归不同单元;胸腺肽中胸腺肽α和胸腺肽F归不同单元。(3)主要化学成分相同,命名中盐基、酸根、碱基、金属元素、晶型、结晶水数量、溶媒、包装、储藏条件不同的药品归同一单元。但特殊情况除外,如可使药品的临床疗效发生实质性改善,经专家论证同意后,可归不同单元。(4)带有附加装置(如加药器、冲洗器、附带溶媒、预灌封或预充式注射器等)的药品,不作为划分单元的依据。但胰岛素制剂中笔芯和非笔芯归不同单元;特充、预充和普通包装胰岛素归不同单元。(5)附带注射溶媒原则上不作划分单元的依据。但溶媒为专用溶媒,且在临床使用上产生重大差别的药品,经专家论证同意后,可作为划分不同单元的依据。(6)主要成分含牛黄或麝香的品种,按天然(含体内培植、体外培育)与人工归不同单元。应有国家食品药品监督管理(总)局生产批件和药品说明书载明。(7)相同通用名,临床适应症完全不同的归不同单元。(8)复方制剂和单方制剂为不同单元;组成成分不同的复方制剂、组方不同的中成药制剂(包括同名异方)归不同单元;组成成分相同的复方制剂、组方相同的中成药制剂(包括同方异名)归同一单元。(9)单支(瓶)剂量相同、容量不同的小容量注射液归为同一单元。(10)大容量注射液按玻璃瓶、塑料瓶、单阀非PVC软袋、双阀非PVC软袋、单阀直立式软袋、双阀直立式软袋包装归为不同单元;小容量注射液包装按照玻璃、塑料等材质归不同单元。(11)肌注与静注归不同单元,既可肌注又可静注的归入静注单元;静注与静滴不再划分单元。以上未尽或未涉及事宜由评审委员会论证决定。21
二、《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》补充挂网单元划分规则。宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》补充挂网采购化学药品和生物制品剂型以《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》凡例名称与剂型划分规则为准;中成药品剂型划分规则参考《宁夏回族自治区公立医院药品补充直接挂网采购目录》单元划分规则。附件:宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)凡例《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》(简称《药品目录》)是我区基本医疗保险、工伤保险和生育保险基金支付药品费用的标准。临床医师根据病情开具处方、参保人员购买与使用药品不受《药品目录》的限制。“凡例”是对《药品目录》中药品的分类与编号、名称与剂型、备注等内容的解释和说明,是《药品目录》的组成部分,其内容与目录正文具有同等政策约束力。一、目录构成(一)《药品目录》西药部分和中成药部分所列药品为基本医疗保险、工伤保险和生育保险基金准予支付费用的药品,共2729个,包括西药1372个,中成药1357个(含民族药98个)。其中仅限工伤保险基金准予支付费用的品种6个;仅限生育保险基金准予支付费用的品种4个。36个国家谈判药品及我区新增的4个品种执行差异化支付政策。(二)《药品目录》收载的西药甲类药品402个,中成药甲类药品192个,其余为乙类药品。基本医疗保险基金支付药品费用时区分甲、乙类,工伤保险和生育保险支付药品费用时不分甲、乙类。二、编排与分类(三)药品分类及分类代码执行《社会保险药品分类与代码》行业标准。药品分类西药主要依据解剖-治疗-化学分类(ATC),中成药主要依据功能主治分类。临床具有多种治疗用途的药品,选择其主要治疗用途分类。临床医师依据病情用药,不受《药品目录》分类的限制。(四)西药、中成药分别按药品品种编号。同一品种只编一个号,重复出现时标注“★”,并在括号内标注该品种编号。药品排列顺序及编号的先后次序无特别含义。三、名称与剂型(五)除在“备注”一栏标有“◇”的药品外,西药名称采用中文通用名,未包括命名中的盐基、酸根部分,剂型单列。中成药名称采用中文通用名,剂型不单列。为使编排简洁,在甲乙分类、给药途径、备注相同的情况下,同一通用名称下的不同剂型并列,其先后次序无特别含义。(六)西药剂型在《中国药典》“制剂通则”的基础上合并归类处理,未归类的剂型以《药品目录》标注的为准。合并归类的剂型所包含的具体剂型见下表:合并归类的剂型包含的具体剂型21
口服常释剂型普通片剂(片剂、肠溶片、包衣片、薄膜衣片、糖衣片、浸膏片、分散片、划痕片)、硬胶囊、软胶囊(胶丸)、肠溶胶囊缓释控释剂型缓释片、缓释包衣片、控释片;缓释胶囊、控释胶囊口服液体剂口服溶液剂、口服混悬剂、干混悬剂、口服乳剂、胶浆剂、口服液、乳液、乳剂、胶体溶液、合剂、酊剂、滴剂、混悬滴剂、糖浆剂(含干糖浆剂)丸剂丸剂、滴丸颗粒剂颗粒剂、肠溶颗粒剂口服散剂散剂、药粉、粉剂外用散剂散剂、粉剂、撒布剂、撒粉软膏剂软膏剂、乳膏剂、霜剂、糊剂、油膏剂贴剂贴剂、贴膏剂、膜剂、透皮贴剂外用液体剂外用溶液剂、洗剂、漱口剂、含漱液、胶浆剂、搽剂、酊剂、油剂硬膏剂硬膏剂、亲水硬膏剂凝胶剂乳胶剂、凝胶剂涂剂涂剂、涂膜剂、涂布剂栓剂栓剂、肛门栓、阴道栓滴眼剂滴眼剂、滴眼液滴耳剂滴耳剂、滴耳液滴鼻剂滴鼻剂、滴鼻液吸入剂喷剂、气雾剂、喷鼻剂、喷粉剂、喷雾剂、雾化吸入剂、雾化混悬液、雾化溶液剂、雾化吸入液、吸入性粉剂、干粉剂、干粉吸入剂、粉末吸入剂、干粉吸剂、吸入性溶液剂、吸入性混悬液注射剂注射剂、注射液、注射用溶液剂、静脉滴注用注射液、注射用混悬液、注射用无菌粉末、静脉注射针剂、水针、注射用乳剂、乳状注射液、粉针剂、针剂、无菌粉针、冻干粉针中成药剂型中,丸剂包括水丸、蜜丸、水蜜丸、糊丸、浓缩丸和微丸,不含滴丸;胶囊剂是指硬胶囊,不含软胶囊;其他剂型没有归并。(七)《药品目录》收载的药品不区分商品名、规格或生产厂家。通用名称中主要化学成分部分与《药品目录》中的名称一致且剂型相同,而酸根或盐基不同的西药,属于《药品目录》的药品。21
(八)“备注”栏标有“◇”的药品,因其组成和适应症类似而进行了归类,所标注的名称为一类药品的统称。具体如下:1.西药部分第112号“短效胰岛素类似物”包括:赖脯胰岛素、重组赖脯胰岛素、门冬胰岛素、谷赖胰岛素。2.西药部分第115号“人中效胰岛素”包括:精蛋白锌重组人胰岛素、精蛋白重组人胰岛素、精蛋白生物合成人胰岛素。3.西药部分第117号“普通胰岛素预混”包括:精蛋白锌胰岛素(30R)、精蛋白生物合成人胰岛素(预混30R)、精蛋白重组人胰岛素混合(40/60)、精蛋白锌重组人胰岛素混合、精蛋白重组人胰岛素混合(50/50)、精蛋白重组人胰岛素混合(30/70)、精蛋白重组人胰岛素(预混30/70)、精蛋白生物合成人胰岛素(预混50R)、50/50混合重组人胰岛素、30/70混合重组人胰岛素。4.西药部分第118号“胰岛素类似物预混”包括:门冬胰岛素50、门冬胰岛素30、精蛋白锌重组赖脯胰岛素混合(25R)、精蛋白锌重组赖脯胰岛素混合(50R)。5.西药部分第121号“长效胰岛素类似物”包括:甘精胰岛素、重组甘精胰岛素和地特胰岛素。6.西药部分第174号“缓解消化道不适症状的复方OTC制剂”包括的品种见下表:序号药品名称序号药品名称1复方丙谷胺西咪替丁片19复方胰酶散2复方颠茄铋镁片20复合乳酸菌胶囊3复方颠茄氢氧化铝片21盖胃平片4复方颠茄氢氧化铝散22海藻酸铝镁颗粒5复方淀粉酶口服溶液23硫糖铝小檗碱片6复方雷尼替丁胶囊24龙胆碳酸氢钠片(健胃片)7复方龙胆碳酸氢钠片25龙胆碳酸氢钠散8复方芦荟维U片26铝镁颠茄片9复方木香铝镁片27铝镁混悬液10复方木香小檗碱片28铝镁加混悬液11复方尿囊素片29神黄钠铝胶囊12复方嗜酸乳杆菌片30鼠李铋镁片13复方碳酸钙咀嚼片31碳酸钙甘氨酸胶囊14复方维生素U胶囊32维U颠茄铝胶囊15复方胃蛋白酶颗粒33维U颠茄铝胶囊Ⅱ16复方消化酶胶囊34维U颠茄铝镁胶囊1735维U颠茄铝镁片21
复方溴丙胺太林铝镁片18复方延胡索氢氧化铝片36维U颠茄铝镁片Ⅱ7.西药部分第739号“抗艾滋病用药”是指国家免费治疗艾滋病方案内的药品。8.西药部分第961号“动物骨多肽制剂”包括:骨肽、骨肽(Ⅰ)、鹿瓜多肽和骨瓜提取物。9.西药部分第1157号“青蒿素类药物”是指卫生部《抗疟药使用原则和用药方案》中所列的以青蒿素类药物为基础的处方制剂、联合用药的药物和青蒿素类药物注射剂。10.西药部分第1226号“缓解感冒症状的复方OTC制剂”包括的品种见下表:序号药品名称序号药品名称1氨酚咖黄烷胺片48复方氨酚烷胺胶囊2氨酚美伪滴剂49复方氨酚烷胺颗粒3氨酚那敏三味浸膏胶囊50复方氨酚烷胺片4氨酚烷胺咖敏胶囊51复方北豆根氨酚那敏片5氨酚烷胺那敏胶囊52复方贝母氯化铵片6氨酚伪麻胶囊53复方酚咖伪麻胶囊7氨酚伪麻咀嚼片54复方甘草氯化铵糖浆8氨酚伪麻颗粒剂55复方甘草浙贝氯化铵片9氨酚伪麻美芬胶囊56复方氯丙那林鱼腥草素钠片10氨酚伪麻美芬片57复方枇杷氯化铵糖浆11氨酚伪麻美芬片(Ⅱ)58复方氢溴酸右美沙芬胶囊12氨酚伪麻美芬片(Ⅱ)/苯酚伪麻片59复方氢溴酸右美沙芬糖浆13氨酚伪麻美芬片(Ⅲ)60复方忍冬藤阿司匹林片14氨酚伪麻那敏胶囊61复方锌布颗粒剂15氨酚伪麻那敏胶囊(夜用)62复方盐酸伪麻黄碱缓释胶囊16氨酚伪麻那敏咀嚼片63复方银翘氨敏胶囊17氨酚伪麻那敏分散片64复方愈创木酚磺酸钾口服溶液1865复方愈酚喷托那敏糖浆21
氨酚伪麻那敏分散片(Ⅲ)19氨酚伪麻那敏片66咖酚伪麻片20氨酚伪麻那敏溶液67科达琳21氨酚伪麻片68柳酚咖敏片22氨金黄敏颗粒69洛芬葡锌那敏片23氨咖黄敏胶囊70美尔伪麻溶液24氨咖黄敏口服溶液71美酚伪麻片25氨咖黄敏片72美敏伪麻口服液26氨咖麻敏胶囊73美愈伪麻胶囊27氨咖愈敏溶液74美愈伪麻口服溶液28氨麻苯美片75美愈伪麻口服液29氨麻美敏口服溶液76喷托维林氯化铵片30氨麻美敏片77喷托维林氯化铵糖浆31氨麻美敏片(Ⅱ)78扑尔伪麻片32氨麻美敏片(Ⅲ)79双分伪麻胶囊33贝敏伪麻片80双扑伪麻片34布洛伪麻分散片81双扑伪麻胶囊35布洛伪麻胶囊82双扑伪麻颗粒36布洛伪麻颗粒剂83伪麻那敏胶囊37布洛伪麻片84伪麻那敏片38酚咖麻敏胶囊85右美沙芬愈创甘油醚糖浆39酚咖片86愈创维林那敏片40酚麻美敏胶囊87愈酚喷托异丙嗪颗粒41酚麻美敏片88愈酚维林片42酚麻美软胶囊89愈酚伪麻颗粒43酚美愈伪麻口服液90愈酚伪麻片44酚明伪麻片91愈美胶囊45复方氨酚美沙糖浆92愈美颗粒剂46复方氨酚那敏颗粒93愈美片47复方氨酚葡锌片11.西药部分第1324号“肠内营养剂”包括:肠内营养粉剂(AA-PA)、肠内营养粉剂(AA)、短肽型肠内营养剂、整蛋白型肠内营养剂(粉剂)、肠内营养混悬液Ⅱ21
(TP)、肠内营养混悬液(TPSPA)、肠内营养混悬液(TP-MCT)、肠内营养乳剂(TP-HE)、肠内营养乳剂(TPF-T)、肠内营养混悬液(TPF-FOS)、肠内营养混悬液(TPF-DM)、肠内营养乳剂(TPF-D)、肠内营养混悬液(TPF-D)、肠内营养乳剂(TPF)、肠内营养混悬液(TPF)、肠内营养乳剂(TP)、肠内营养混悬液(TP)、肠内营养粉剂(TP)、肠内营养混悬液(SP)。12.中成药部分第402号“虫草菌发酵制剂”包括:百令片、百令胶囊、金水宝片、金水宝胶囊、宁心宝胶囊、至灵胶囊。13.中成药部分第510号“薯蓣皂苷口服制剂”包括:地奥心血康片、地奥心血康颗粒、地奥心血康软胶囊、薯蓣皂苷片。14.中成药部分第556号“三七皂苷注射制剂”包括:血塞通注射液、血栓通注射液、注射用血塞通(冻干)、注射用血栓通(冻干)。15.中成药部分第561号的“灯盏注射制剂”包括:灯盏细辛注射液、灯盏花素注射液、注射用灯盏花素。16.中成药部分第569号“三七皂苷口服制剂”包括:三七通舒胶囊、血塞通片、血塞通胶囊、血塞通颗粒、血塞通软胶囊、血栓通胶囊。17.中成药部分第579号的“银杏叶口服制剂”包括:银杏叶滴丸、银杏叶胶囊、银杏叶颗粒、银杏叶口服液、银杏叶片、银杏叶丸、银杏叶提取物滴剂、银杏叶提取物片、银杏酮酯滴丸、银杏酮酯胶囊、银杏酮酯颗粒、银杏酮酯片、银杏酮酯分散片、杏灵分散片、银杏蜜环口服溶液。18.中成药部分第580号“银杏叶注射制剂”包括:银杏达莫注射液、银杏叶注射液、银杏叶提取物注射液、注射用银杏叶提取物、舒血宁注射液。19.中成药部分第833号的“复方红曲口服制剂”包括:血脂康片、脂必妥片、脂必妥胶囊、脂必泰胶囊。20.中成药部分第1198号的“狗皮膏制剂”包括:狗皮膏、狗皮膏(改进型)、精制狗皮膏、新型狗皮膏。四、限定支付范围(九)医疗保险统筹基金支付《药品目录》内药品所发生的费用,必须由医生开具处方或住院医嘱,参保患者自行购买药品发生的费用,由个人账户支付或个人自付。儿童或有临床证据证明为智力障碍的成人参保人员,由医生处方或住院医嘱使用与目录药品名称和剂型相同的非处方药品发生的费用,可以由统筹基金按规定支付。(十)“备注”栏中对部分药品规定了限定支付范围,是指符合规定情况下参保人员发生的药品费用,可按规定由基本医疗保险或生育保险基金支付,工伤保险支付药品费用时不受限定支付范围限制。经办机构在支付费用前,应核查相关证据。1.“备注”一栏标有“△”的药品,是参保人员住院使用时由基本医疗保险统筹基金按规定支付,门诊使用时由职工基本医疗保险个人账户支付的药品。2.“备注”一栏标为“限工伤保险”21
的药品,是仅限于工伤保险基金支付的药品,不属于基本医疗保险、生育保险基金支付范围。3.“备注”一栏标为“限生育保险”的药品,是仅限于生育保险基金支付的药品,不属于基本医疗保险、工伤保险基金支付范围。4.“备注”一栏标注了适应症的药品,是指参保人员出现适应症限定范围情况并有相应的临床体征及症状、实验室和辅助检查证据以及相应的临床诊断依据,使用该药品所发生的费用可按规定支付。适应症限定不是对药品法定说明书的修改,临床医师应根据病情合理用药。5.“备注”一栏标注了二线用药的药品,支付时应有使用《药品目录》内一线药品无效或不能耐受的证据。(十一)国家免费治疗艾滋病方案内的药品,不属于国家免费治疗艾滋病范围的参保人员使用治疗艾滋病时,基本医疗保险基金可按规定支付费用。国家公共卫生项目涉及的抗结核病和抗血吸虫病药物,不属于国家公共卫生支付范围的参保人员使用时,基本医疗保险基金可按规定支付费用。(十二)参保人员使用西药部分第257-272号“胃肠外营养液”、第289号“丙氨酰谷氨酰胺注射剂”、第1324号“肠内营养剂”,需经营养风险筛查明确具有营养风险时方可按规定支付费用。使用肠外或肠内营养支持疗法时,消化道有功能的患者应首先选用肠内营养剂。五、其他(十三)中成药部分药品处方中含有的“麝香”是指人工麝香,“牛黄”是指人工牛黄、体内培植牛黄和体外培育牛黄。关于医保目录剂型填报的补充说明:医保目录中成药的剂型填报按照宁夏回族自治区公立医院药品补充直接挂网采购目录单元划分规则中的剂型选择填报,若剂型选择中无企业药品相关剂型,企业可自行添加。二、《中国上市药品目录集》药品单元划分规则,参照《宁夏回族自治区公立医院药品补充直接挂网采购目录》单元划分规则。第四部分药品补充直接挂网采购目录一、《2018年宁夏回族自治区公立医院补充直接挂网采购药品目录》;二、《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》补充直接挂网目录;三、《中国上市药品目录集》补充直接挂网目录。21
目录说明:1.依据《自治区物价局关于低价药品价格管理有关问题的通知》(宁价费发﹝2018﹞9号)精神,本次直接挂网采购目录不再设定低价药品目录。以药品实际交易价格计算,凡符合低价药品日均费用标准的(西药不超过3元、中成药不超过5元),可按照国家低价药品相关规定和我区药品集中采购相关规定,开展低价药品采购工作,确保低价药品供应;凡不符合低价药品日均费用标准的,不得执行低价药品相关政策。药品生产经营企业可自行选择是否进入或退出低价药品管理,并保持价格相对稳定。2.收录在《中国上市药品目录集》中的药品生产企业及其药品品规,未取得宁夏回族自治区公立医院药品集中采购中标(挂网、成交)资格的药品生产企业及其药品品规。由药品生产企业自主申报药品的药品通用名、剂型、规格、批准文号(或注册证号)、参比制剂、标准制剂、上市许可持有人等信息。申报信息应与《中国上市药品目录集》中的信息一致。系统已经内置《中国上市药品目录集》药品,相关企业可直接选择进行企业和药品资质的维护;部分未收录在中国上市药品目录集中的通过或视同通过仿制药一致性评价的药品,企业需自行添加药品通用名、剂型、规格等相关信息后,再进行维护企业和药品相关信息。通过或视同通过仿制药质量和疗效一致性评价的药品,需提交国家食品药品监督管理总局核发批准证明文件。3.《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》中未纳入《2015年宁夏回族自治区公立医院药品招标采购目录》和《2016年宁夏回族自治区公立医院直接挂网采购药品目录》的药品品规,由药品生产企业自主申报药品通用名、剂型和规格。药品通用名和剂型应符合《自治区人力资源社会保障厅关于印发宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)的通知》的规定。国家谈判药品仿制药属基本医疗保险、工伤保险和生育保险药品目录范围。4.若企业申报的药品在《2018年宁夏回族自治区公立医院补充直接挂网采购药品目录》和《宁夏回族自治区基本医疗保险、工伤保险和生育保险药品目录(2017年版)》补充直接挂网目录中均存在,请企业选择《2018年宁夏回族自治区公立医院补充直接挂网采购药品目录》中的药品填报。21
第五部分企业申报文件参考格式33
项目名称:2018年宁夏回族自治区公立医院药品补充直接挂网(NYC/YP201802)申报文件企业名称:(盖单位章)法定代表人或其委托代理人:(签字)联系电话:年月日33
目录1、申报函2、企业基本情况说明3、生产企业法定代表人授权书4、进口药品生产企业授权委托书5、申报药品基本信息表6、药品供货承诺函7、企业资质证明文件8、药品资质证明文件33
1、申报函2018年宁夏回族自治区公立医院药品补充直接挂网申报函(采购编号:NYC/YP201802)致:宁夏药品统一招标采购领导小组办公室:在审阅了本次《2018年宁夏回族自治区公立医院药品补充直接挂网采购文件》(采购编号:NYC/YP201802)后,我方决定按照本次发布的采购文件申报,现承诺如下:(1)我方同意以《采购文件》要求的药品信息及确定的药品价格参与采购活动。我方保证所提供的全部报价和其它资质证明文件真实、完整和合法,并愿赔偿贵方因上述报价和资质证明文件的缺陷所蒙受的全部经济损失及承担相应的法律责任。(2)如果我方申报药品成交,我方将按照医疗机构的要求按时交付成交药品,确保药品购销合同的履行。(3)我方同意本申报函在采购公告规定的开标之日起120日内有效,并对我方具有约束力。(4)我方承诺,不在2018年宁夏回族自治区公立医院药品补充直接挂网采购活动中有任何违法违规行为,并严格按照网上操作要求进行信息维护及价格申报。(5)在正式合同签订前,本申报函及贵方的“挂网结果公示”将构成约束我们双方的合同。我方完全理解贵方不一定要接受最低报价的挂网。(6)我方严格按申报函附件中的承诺对医疗机构进行服务。申报企业(盖章):法定代表人(签字):出具日期:年月日33
申报函附件:申报企业(盖章):申报企业伴随服务承诺(包括破损退换、近效期退换等)A、承诺及时补给合格药品或退货。()B、不做上述承诺。()必须用“√”确认承诺,否则将不得分。注意:申报企业必须谨慎选择、填写,作为申报文件的重要组成部分,中标人必须在采购期的履约过程中严格遵守。33
2、企业基本情况说明企业基本情况说明(采购编号:NYC/YP201802)申报企业名称(公章)______________________法人代表(签字)___________申报企业所在地_________________________________联系电话_______________________传真_______________________通信地址______________________________________邮政编码___________电子信箱___________开户银行______________________________________开户帐号______________________________________需要说明的其他信息_____________________________兹证明上述声明是真实、准确的,并提供了全部能够提供的资料和数据,我们同意遵照招标机构要求出示有关证明文件。33
3、生产企业法定代表人授权书2018年宁夏回族自治区公立医院药品补充直接挂网法定代表人授权书(采购编号:NYC/YP201802)本授权书声明:注册于(公司地址)的(公司名称)的(法定代表人姓名、职务)代表本公司授权(被授权人的姓名、职务)(身份证号)为公司的唯一合法代理人,就2018年宁夏回族自治区公立医院药品补充直接挂网采购活动中报名、领取采购文件、用户名及密码、提交申报文件、确认申报相关信息及药品购销合同的签订、执行、完成和售后服务,以本公司名义处理一切与之有关的事务。我方郑重承诺:成交后我企业将无条件按照挂网品种的规格、剂型、包装在交易期内保证药品的货源和质量,如有违反,依据《中华人民共和国招标投标法》、《中华人民共和国合同法》、《药品集中招标采购监督管理办法》(国纠办发〔2010〕6号)、《宁夏回族自治区医疗机构药品招标采购“三统一”监督管理特别规定(试行)》(宁政发〔2007〕115号)、《宁夏回族自治区人民政府办公厅关于完善宁夏公立医院药品集中采购工作的实施意见》(宁政办发〔2015〕142号)等文件同时承诺:(1)我方提交的报价是我方慎重考虑的结果,一经提出,即为要约。任何违反行为,我方都将接受宁夏药品统一招标领导小组根据国家和宁夏相关法律法规做出的处罚。(2)如我方出现不履约的行为,我方愿意接受宁夏药品统一招标领导小组办公室作出的,最多为三年之内不得参加宁夏药品统一采购的附加处罚。本授权书于年月日签字生效,特此声明。授权人(法定代表人)签字(盖章)被授权人签字(盖章)单位名称地址代理人(被授权人)居民身份证复印件反面代理人(被授权人)居民身份证复印件正面加盖企业公章33
4、进口药品(或生产企业集团公司所属销售公司)药品生产企业授权书2018年宁夏回族自治区公立医院药品补充直接挂网进口药品生产企业授权书致:宁夏药品统一招标采购领导小组办公室作为生产下表所列药品的____________________________(生产企业全称),根据本次《2018年宁夏回族自治区公立医院药品补充直接挂网采购文件》(采购编号:NYC/YP201802)的规定:同一生产厂家的品种申报企业仅限1家,我企业在此授权____________________________(药品经营企业,生产企业集团公司所属销售公司只投报本集团公司所属分厂生产的药品)作为独家代理企业,用我厂(公司)生产的产品参加本次药品补充公开招标采购活动,递交申报函并签署购销合同。我厂(公司)郑重承诺:成交后我企业将无条件按照挂网品种的规格、剂型、包装在交易期内保证药品的货源和质量,如有违反,依据《中华人民共和国招标投标法》、《中华人民共和国合同法》、《药品集中招标采购监督管理办法》(国纠办发〔2010〕6号)及《宁夏回族自治区医疗机构药品招标采购“三统一”监督管理特别规定(试行)》(宁政发〔2007〕115号)、《自治区政府办公厅关于印发宁夏回族自治区基本药物统一招标(采购)实施办法的通知》(宁政办发〔2011〕7号)承担法律责任。授权期限为:年月起至本次中标药品采购期结束。购销合同规定的挂网采购期限与本授权书的有效期限应一致。若购销合同规定的挂网采购期限延期,本授权书期限自动顺延到挂网采购期限届满。此授权书一经授出,在挂网截止期后将不作任何修改。药品生产企业名称(盖章)进口药品独家代理企业名称(盖章)联系电话、传真:法定代表人(签字)日期:年月日(加盖申报企业公章)33
5、申报药品基本信息表申报药品基本信息表(含申报报价)编号产品目录序号YPID通用名剂型规格转换系数最小制剂单位最小包装单位包装最小制剂单位申报价格(元)最小包装申报价格(元)生产企业名称备注企业名称(盖章)日期:年月日(加盖企业公章)注:(1)本表必须打印,不得手写(法人代表人签字除外),不得行间插字和涂改,如有涂改,必须有生产厂家在涂改处加盖公章。(2)对品种通用名、剂型、制剂规格、包装规格的描述应与采购文件品种信息一致,且申报品种序号必须与本采购文件中的产品目录序号相一致。按照产品目录序号从小到大顺序书写。33
6、药品供货承诺函2018年宁夏回族自治区公立医院药品补充直接挂网药品供货承诺函(委托“统一配送”企业配送)(采购编号:NYC/YP201802)宁夏药品统一招标领导小组办公室:我单位_______________________(企业名称)是合法注册的药品生产企业。在此承诺:我单位参加本次药品直接挂网品种的所有药品一旦成交(以下同),我方按照工作要求,委托“统一配送”企业进行配送工作。我方愿积极配合“统一配送”单位,并承担对本次挂网采购药品的供应。我方保证中标后,严格按照本次《2018年宁夏回族自治区公立医院药品补充直接挂网采购文件》及采购方的要求,及时供货并提供全面、完善的服务。同时承诺:如我方出现故意不履约的行为,我方愿意接受宁夏药品统一招标领导小组办公室作出的,最多为两年之内不得参加宁夏药品统一采购的附加处罚。本承诺书有效期限:自签订购销合同开始至本次补充直接挂网采购药品采购交易有效期截止。购销合同规定采购期限与本承诺书的有效期限应一致。若购销合同规定的采购期限延期,本承诺期限自动顺延到采购期限届满。特此承诺。申报企业名称(盖章):___________________________________法定代表人(签字):__________________联系人:____________________________联系电话:____________________________日期:_________年___月___日33
7、企业资质文件封面企业资质文件申报企业名称:联系人:联系电话:电子邮件:33
8、药品资质证明文件封面挂网目录中药品序号药品YPID码药品目录通用名申报药品说明书标注名称(实际通用名)药品目录剂型说明书中具体剂型(实际剂型)药品目录规格说明书中具体规格(实际规格)其他说明:说明书中具体剂型指剂型的细化分类。如申报药品是片剂,需在说明书中具体剂型一栏注明是素片、包衣片、糖衣片、薄膜衣片、划痕片、浸膏片、分散片、肠溶片等。33'
您可能关注的文档
- 本科毕业生登记表(样本)
- 山西高职院校单独招生考生报名登记表
- 107年奈米中心1~2月施工登记表
- 岐山第十八届人大一次会议期间代表议案建议登记表
- 北京市残疾人证申领审批登记表
- 医疗废物暂存站消毒登记表,
- 特种设备使用登记表
- 暑期社会实践登记表
- 行政服务事项登记表及流程图共7项
- 伊金霍洛旗行政审批事项前置条件情况登记表
- 毕业生登记表班级鉴定-毕业生登记表班级鉴定 毕业生登记表班级意见
- 江苏高等教育考生报名登记表
- 2010年度姜堰企业技术难题需求项目信息登记表
- 入河排污口登记表
- 我国民航大学大学毕业生登记表
- 2018年阳光使者国际派遣生报名登记表
- 济南大学2015年辅导员岗位报名登记表
- 东门街道办事处行政检查事项登记表及流程图共4项