- 1.28 MB
- 2022-04-29 14:29:21 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'原电池原理及其应用
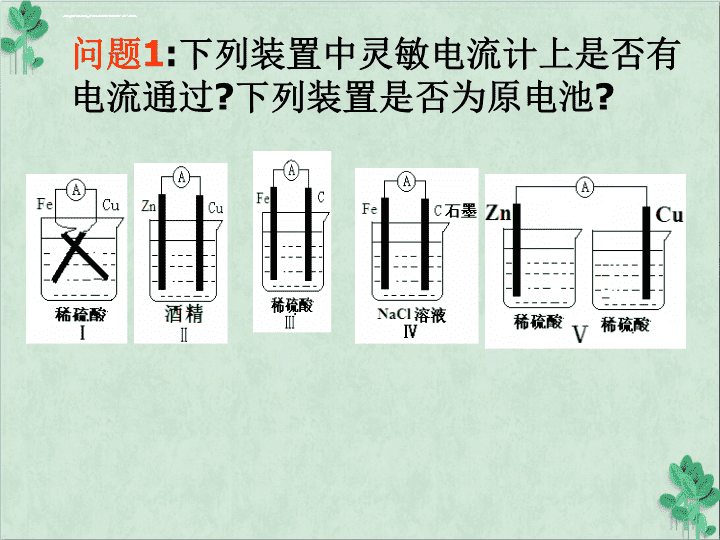
问题1:下列装置中灵敏电流计上是否有电流通过?下列装置是否为原电池?
构成原电池条件①电解质溶液②活泼性不同的两电极③形成闭合回路
问题2:有电流说明有电能产生,电能是怎样转化来的?例1、Zn、Cu作两极,稀硫酸作电解质溶液的原电池中:①Cu作____极,②Zn作____极电极反应式是:负极___________,正极_____________,总反应式是___________________________正负Zn-2e-=Zn2+2H++2e-=H2↑Zn+H2SO4=ZnSO4+H2↑
1、原电池的反应原理自发进行的氧化还原反应化学能转化为电能2、原电池电极的判断负极—相对活泼-失电子-电子流出-发生氧化反应正极—相对不活泼-得电子-电子流入-发生还原反应3.离子移动方向:阳离子正极,阴离子负极
知识拓展:原电池是由两个半电池组成的;半电池包括电极材料和电解质溶液,两个隔离的半电池通过盐桥连接起来。半电池中的反应就是半反应即电极反应。所以半电池又叫电极。
盐桥:在U型管中装满用饱和KCl溶液和琼脂做成的冻胶。这种装置能将化学能转变为电能,称为原电池(PrimaryCell)盐桥的作用:使Cl-向锌盐方向移动,K+向铜盐方向移动,使Zn盐和Cu盐溶液一直保持电中性,从而使电子不断从Zn极流向Cu极。这样可以大大提高电池效率。
原电池电极反应式的书写注意事项:(1)找出两极放电的物质,负氧正还。(2)要注意溶液的酸碱性,适当的在电极方程式两边添加H+、OH—、H2O,以遵循电荷守恒和质量守恒。(3)要注意电极反应产物是否与电解质溶液发生反应。小结
原电池应用负极(锌筒):Zn-2e-=Zn2+正极(石墨):2NH4++2e-=2NH3↑+2H2↑总反应:Zn+2NH4+=Zn2++2NH3↑+2H2↑1、锌-锰干电池(酸性)常用电池的电极反应和电池总反应式书写
2、铅蓄电池负极Pb:Pb+SO42--2e-=PbSO4正极PbO2:PbO2+4H++SO42-+2e-=PbSO4+2H2O总反应:
钮扣电池:不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极一端填充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为浓KOH溶液,已知电池内Zn的氧化产物为ZnO,3、银-锌电池负极:Zn+2OH--2e-=ZnO+H2O正极:Ag2O+H2O+2e-=2Ag+2OH-总反应:Ag2O+Zn=ZnO+2Ag
电极:Pt制作的惰性电极电解质溶液:KOH溶液负极:2H2-4e-+4OH-=4H2O正极:O2+2H2O+4e-=4OH-总反应:2H2+O2=2H2O拓展创新氢氧燃料电池若为酸性介质,试写出电极反应式?思考:负极:2H2-4e-=4H+正极:O2+4H++4e-=2H2O4、新型燃料电池(氢氧燃料电池/甲烷电池/煤气电池/海水-空气电池)
5、海水电池(电解质溶液为海水)负极:4Al-12e—=4Al3+,正极:3O2+6H2O+12e—=12OH—总反应:4Al+3O2+6H2O=4Al(OH)36、锂电池(非水有机溶剂电解液)负极:2Li-2e—=2Li+,正极:I2+2e—=2I—,总反应:2Li+I2=2LiI跟相同质量的其它金属作负极相比,使用寿命延长,高能、质轻、电压高、工作效率高、储存寿命长。
1、2、金属阳离子失e-氧化反应金属腐蚀的类型化学腐蚀电化腐蚀析氢腐蚀吸氧腐蚀(常见普遍)金属腐蚀及防护金属原子金属腐蚀的本质:3、金属腐蚀:是指金属或合金跟接触的气体或液体发生化学反应(氧化—还原)而腐蚀损耗的过程。
钢铁表面形成的微小原电池示意图钢铁的腐蚀
钢铁的析氢腐蚀示意图钢铁的吸氧腐蚀示意图
Fe2O3·nH2O(铁锈)通常两种腐蚀同时存在,但以后者更普遍。析氢腐蚀吸氧腐蚀条件水膜呈酸性。水膜呈中性或酸性很弱。CO2+H2OH2CO3H++HCO3-电极反应负极Fe(-)Fe-2e=Fe2+2Fe-4e=2Fe2+正极C(+)2H++2e=H2↑O2+2H2O+4e=4OH-总反应:Fe+2H+=Fe2+↑2Fe+2H2O+O2=2Fe(OH)24Fe(OH)2+2H2O+O2=4Fe(OH)3联系
钢铁腐蚀的防护:例6:改变金属的内部组织结构:如将Cr、Ni等金属加进钢里制成合金钢。⒈A.C.铜的金属活动性比氢小,因此不宜被氧化;B.D.它们的表面都电镀上了一层耐腐蚀的黄金;2000年5月,保利集团在香港拍卖会上花费3000多万港币购回在火烧圆明园时流失的国宝:铜铸的牛首、猴首和虎首,普通铜器时间稍久容易出现铜绿,其主要成分是[Cu2(OH)2CO3]这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对起原因的分析,最可能的是环境污染日趋严重,它们表面的铜绿被酸雨溶解洗去;(D)它们是含一定比例金、银、锡、锌的合金;
2.金属表面覆盖保护层3.电化学保护法原理:原理:如油漆、油脂等,电镀(Zn,Cr等易氧化形成致密的氧化物薄膜)作保护层。隔绝金属与外界空气、电解质溶液的接触。——牺牲阳极的阴极保护法形成原电池反应时,让被保护金属做正极,不反应,起到保护作用;而活泼金属反应受到腐蚀。
牺牲阳极的阴极保护法示意图
练习:下列装置中的纯锌棒都浸在相同浓度的稀硫酸中,锌棒腐蚀速度从快到慢的顺序是A③④②①B②③①④C④②①③D③②①④D
在同一电解质溶液中,金属腐蚀的快慢规律如下:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐措施的腐蚀防腐措施由好到坏的顺序如下:外接电源的阴极保护法>牺牲阳极的阴极保护法>有一般防腐条件的腐蚀>无防腐条件的腐蚀小结
例1:航天技术上使用的氢氧燃料电池具有高能、轻便、无污染的优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应都可以表示为2H2+O2=2H2O,酸式电池中电解质是酸,其负极反应可表示为____________,则其正极反应式为_______________。碱式电池的电解质是碱,其正极反应式为__________________,则其负极反应可表示为_________________________。2H2-4e-+4OH-=4H2O2H2-4e-=4H+O2+4e-+4H+=2H2OO2+2H2O+4e-=4OH-
例2:氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出图中甲烷燃料电池中a极的电极反应式:,此时电池内总的反应式。KOH溶液CH4O2H2OabCH4+10OH--8e-=CO32-+7H2OCH4+2O2+2KOH=K2CO3+3H2O
例3:有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是()①每消耗1molCH4可以向外电路提供8mole-②负极上CH4失去电子,电极反应式:CH4+10OH--8e-=CO32-+7H2O③负极上是O2获得电子,电极反应式为:O2+2H2O+4e-=4OH-④电池放电后,溶液PH不断升高A.①②B.①③C.①④D.③④A
例4:已知下列原电池的总反应式,Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应式负极:________________正极:_______________例5:将上题中的反应设计成原电池。画出装置图并注明电极材料及电解质溶液。2Fe3++2e-=2Fe2+Cu-2e-=Cu2+
例6:蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:下列有关爱迪生蓄电池的推断错误的是()A.放电时,Fe是负极,NiO2是正极B.蓄电池的电极可以浸入某中酸性电解质溶液中C.充电时,阴极上的电极反应为:D.放电时,电解质溶液中的阴离子向正极方向移动答案:B、D。
例7、(99理综)熔融盐燃料电池具有高的发电效率,因而受到重视.可用Li2CO3和Na2CO3的熔融盐混合物用电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在6500℃下工作的燃料电池,完成有关的电池反应式:负极反应式:,正极反应式:O2+2CO2+4e=2CO32-总电池反应式:.2CO+2CO32--4e-=4CO22CO+O2=2CO2解析:本题中CO为还原剂,空气中O2为氧化剂,电池总反应式为:2CO+O2==2CO2。用总反应式减去电池负极(即题目指的阳极)反应式,就可得到电池正极(即题目指的阴极)反应式:O2+2CO2+4e-==2CO32-。
4、教学必须从学习者已有的经验开始。——杜威5、构成我们学习最大障碍的是已知的东西,而不是未知的东西。——贝尔纳6、学习要注意到细处,不是粗枝大叶的,这样可以逐步学习摸索,找到客观规律。——徐特立7、学习文学而懒于记诵是不成的,特别是诗。一个高中文科的学生,与其囫囵吞枣或走马观花地读十部诗集,不如仔仔细细地背诵三百首诗。——朱自清8、一般青年的任务,尤其是共产主义青年团及其他一切组织的任务,可以用一句话来表示,就是要学习。——列宁9、学习和研究好比爬梯子,要一步一步地往上爬,企图一脚跨上四五步,平地登天,那就必须会摔跤了。——华罗庚10、儿童的心灵是敏感的,它是为着接受一切好的东西而敞开的。如果教师诱导儿童学习好榜样,鼓励仿效一切好的行为,那末,儿童身上的所有缺点就会没有痛苦和创伤地不觉得难受地逐渐消失。——苏霍姆林斯基11、学会学习的人,是非常幸福的人。——米南德12、你们要学习思考,然后再来写作。——布瓦罗14、许多年轻人在学习音乐时学会了爱。——莱杰15、学习是劳动,是充满思想的劳动。——乌申斯基16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东18、只要愿意学习,就一定能够学会。——列宁19、如果学生在学校里学习的结果是使自己什么也不会创造,那他的一生永远是模仿和抄袭。——列夫·托尔斯泰20、对所学知识内容的兴趣可能成为学习动机。——赞科夫21、游手好闲地学习,并不比学习游手好闲好。——约翰·贝勒斯22、读史使人明智,读诗使人灵秀,数学使人周密,自然哲学使人精邃,伦理学使人庄重,逻辑学使人善辩。——培根23、我们在我们的劳动过程中学习思考,劳动的结果,我们认识了世界的奥妙,于是我们就真正来改变生活了。——高尔基24、我们要振作精神,下苦功学习。下苦功,三个字,一个叫下,一个叫苦,一个叫功,一定要振作精神,下苦功。——毛泽东25、我学习了一生,现在我还在学习,而将来,只要我还有精力,我还要学习下去。——别林斯基13、在寻求真理的长河中,唯有学习,不断地学习,勤奋地学习,有创造性地学习,才能越重山跨峻岭。——华罗庚52、若不给自己设限,则人生中就没有限制你发挥的藩篱。53、希望是厄运的忠实的姐妹。54、辛勤的蜜蜂永没有时间悲哀。55、领导的速度决定团队的效率。56、成功与不成功之间有时距离很短只要后者再向前几步。57、任何的限制,都是从自己的内心开始的。58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。59、不要说你不会做!你是个人你就会做!60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。64、每一个发奋努力的背后,必有加倍的赏赐。65、再冷的石头,坐上三年也会暖。66、淡了,散了,累了,原来的那个你呢?67、我们的目的是什么?是胜利!不惜一切代价争取胜利!68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。70、平凡的脚步也可以走完伟大的行程。71、胜利,是属于最坚韧的人。72、因害怕失败而不敢放手一搏,永远不会成功。73、只要路是对的,就不怕路远。74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。3、上帝助自助者。24、凡事要三思,但比三思更重要的是三思而行。25、如果你希望成功,以恒心为良友,以经验为参谋,以小心为兄弟,以希望为哨兵。26、没有退路的时候,正是潜力发挥最大的时候。27、没有糟糕的事情,只有糟糕的心情。28、不为外撼,不以物移,而后可以任天下之大事。29、打开你的手机,收到我的祝福,忘掉所有烦恼,你会幸福每秒,对着镜子笑笑,从此开心到老,想想明天美好,相信自己最好。30、不屈不挠的奋斗是取得胜利的唯一道路。31、生活中若没有朋友,就像生活中没有阳光一样。32、任何业绩的质变,都来自于量变的积累。33、空想会想出很多绝妙的主意,但却办不成任何事情。34、不大可能的事也许今天实现,根本不可能的事也许明天会实现。35、再长的路,一步步也能走完,再短的路,不迈开双脚也无法到达。'
您可能关注的文档
- 《花的结构和类型》课件PPT课件.ppt
- 《新型玻璃》课件PPT课件.ppt
- 工程机械讲义课件PPT课件.ppt
- 工作礼仪培训课件PPT课件.ppt
- 小学语文一年级上册《汉语拼音教学_a_o_e》教学课件PPT课.ppt
- 对数与对数运算课件PPT-人教版高中数学必修一第二章2.2.1 第二课时.ppt
- 现代文阅读方法教学课件PPT模板下载.pptx
- 国际化经营战略概述课件PPT课件.ppt
- 商务沟通与协调(培训讲座课件PPT).ppt
- 卤代烃、醇和酚 鲁科版(课件PPT).ppt
- 卡通儿童成长教学课件PPT模板.ppt
- 华东理工高等数学(上)11学分课件PPT-2.1 导数的概念.ppt
- 区域农业发展讲义课件PPT课件.ppt
- 北师大版数学二年级下册《买鲜花》2课件PPT版.ppt
- 苏教版五年级科学上册第一单元《3.昼夜交替》优秀课件PPT.pptx
- 统编版八年级语文上册《苏州园林》教学课件PPT模板下载.pptx
- 高中语文人教版《再别康桥》教学课件PPT模板下载.pptx
- 初中语文人教版七年级下册《台阶》教学课件PPT模板下载.pptx