- 550.00 KB
- 2022-04-29 14:28:32 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'水的电离和溶液的酸碱性
常温下,某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,该溶液可能是()①二氧化硫水溶液②氯化铵水溶液③硝酸钠水溶液④氢氧化钠水溶液A.①④ B.①②C.②③ D.③④水的电离和溶液的酸碱性判断
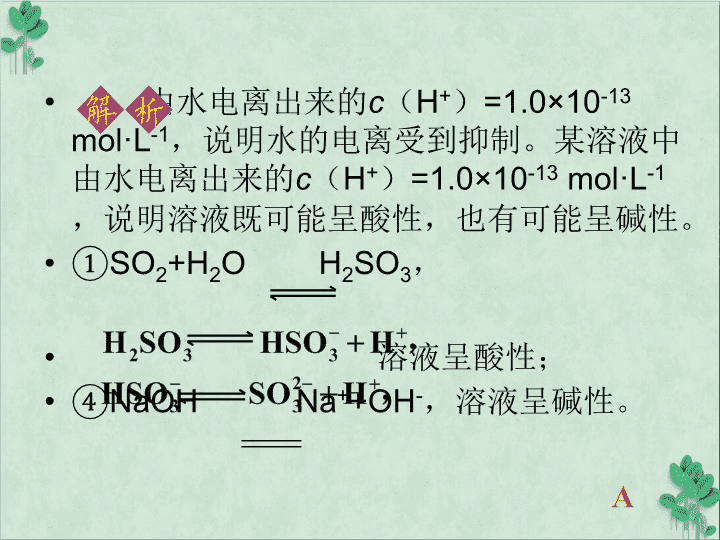
由水电离出来的c(H+)=1.0×10-13mol·L-1,说明水的电离受到抑制。某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,说明溶液既可能呈酸性,也有可能呈碱性。①SO2+H2O H2SO3,溶液呈酸性;④NaOHNa++OH-,溶液呈碱性。A
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是( )
A.水电离的c(H+):①=②=③=④B.将②、③溶液混合后,pH=7,消耗溶液的体积:②>③C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大D.向溶液中加入100mL水后,溶液的pH:③>④>①>②
pH相同即溶液中的氢离子浓度相同。CH3COOH为弱酸,氨水为弱碱,其浓度比0.01mol/L大。AB
1.酸性溶液步骤:先求溶液中氢离子浓度即c(H+),然后求溶液的pH。c(H+)的计算式为:(1)强酸HnA:c(H+)=n×c(酸)(2)强酸稀释:溶液的PH的应用和计算
(3)强酸混合:(4)强酸与强碱混合:
2.碱性溶液步骤:先求出溶液中氢氧根离子浓度即c(OH-),然后根据KW求出溶液中氢离子浓度即c(H+),最后求出溶液的pH。c(OH-)的求算式与酸性溶液中c(H+)的求算式相似,只需把公式中的H+改为OH-,酸改为碱即可。说明:若忽略混合前后溶液体积的变化,则混合后溶液体积近似等于混合前各溶液体积之和,即V混=V1+V2。
将一定体积的NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液的体积为V2;则下列叙述正确的是()
A.若V1>V2,则说明HA的酸性比HB的酸性强B.若V1>V2,则说明HA的酸性比HB的酸性弱C.因为两种酸溶液的pH相等,故V1一定等于V2D.HA、HB分别和NaOH中和反应后,所得的溶液都一定呈中性因为两种酸溶液的pH相等,若HB为弱酸,则其浓度较HA的浓度大,所以消耗的体积较小,即V1>V2。A
t℃时,某稀硫酸溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=13。(1)该温度下水的离子积常数KW的数值为_________________。(2)该温度下(t℃),将100mL0.1mol·L-1的稀H2SO4溶液与100mL0.4mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=________。10-13或1.0×10-1312
1.仪器和试剂滴定管、铁架台(滴定管夹)、锥形瓶、烧杯、标准液和待测液、指示剂2.操作步骤:①检查滴定管是否漏水(操作方法);②蒸馏水洗涤;③标准液或待测液润洗滴定管2~3次;④装液和赶气泡调零;⑤滴定;⑥读数。中和滴定
3.指示剂选用:①变色要灵敏,变色范围要小,且变色范围尽量与所生成盐的溶液酸碱性一致(因此中和滴定一般选用酚酞、甲基橙,而不用石蕊试液)。②强酸滴定强碱一般用甲基橙,但用酚酞也可以。③用酸滴定Na2CO3溶液,酚酞作指示剂,终点产物为NaHCO3和NaCl,而用甲基橙作指示剂终点产物为NaCl、H2O、CO2。
④终点判断
4.数据的记录和处理:数据的记录应精确到小数点后两位,如:24.00mL、23.38mL,最后一位是估计值。滴定至少要做两次,如果两次滴定所耗的标准液的体积相差不到0.20mL,则取两次记录数据的平均值进行计算;如果两次滴定体积相差超过0.20mL,则要继续滴定,直到相邻两次滴定所耗的标准液的体积相差不到0.20mL为止。
5.误差分析:(1)误差分析方法:中和滴定实验中,不同的错误操作引起不同的量的偏差,分析时应注意思维的有序性,首先依题意列出计算式,再区别计算过程中不变量和变化量,然后紧紧抓住变化量对实验结果的影响进行分析。
(c、V、n分别表示溶液物质的量浓度、溶液体积、酸或碱的元数)在实际计算时,标准液浓度和待测液体积按已知数据计算,是不变量。只有滴定管中所消耗的标准溶液体积V(标)随不同操作而变化。从上述计算式可知V(标)与c(待)成正比。以上实验中,只要使V(标)增大的操作所得待测液浓度都偏大。
(2)误差分析结论。造成测定结果偏大的错误操作:滴定管用水润洗后未用标准液润洗就直接注入标准液;滴定前盛标准液的滴定管尖嘴内有气泡,滴定完毕后气泡消失;滴定过程中不慎将标准液滴出锥形瓶外或滴定管漏液;滴定前读数准确,滴定后仰视滴定管刻度;锥形瓶用蒸馏水洗净后再用待测液润洗等。造成测定结果偏低的错误操作:量取待测溶液的滴定管(或移液管)未润洗直接吸取待测液;记录起始体积时仰视读数(或终点时俯视);
用含Na2CO3杂质的NaOH配制标准溶液来测定盐酸浓度等。滴定,不仅仅是酸碱中和滴定,当然也不仅仅用于测定未知溶液的物质的量浓度,只要两种物质在溶液中能够发生反应,而且反应完全时有明显的现象(一般是溶液颜色的变化),都可以称之为滴定。滴定时一般要根据反应物或生成物的性质加入指示剂,但对于反应物或生成物本身就有明显颜色的反应可以不用指示剂,比如有KMnO4参加的反应。
取相同体积(0.025L)的两份0.01mol·L-1NaOH溶液,把其中一份放在空气中一段时间后,溶液的pH________(填“增大”、“减小”或“不变”),其原因是_________________________________________________________。减小因NaOH与空气中CO2反应,造成NaOH减少,故溶液pH减小
用已知浓度的硫酸溶液中和上述两份溶液,其中第一份(在空气中放置一段时间)所消耗硫酸溶液的体积为V(A),另一份消耗硫酸溶液的体积V(B),则:(1)以甲基橙为指示剂时,V(A)和V(B)的关系是___________________;(2)以酚酞为指示剂时,V(A)和V(B)的关系是_____________________。V(A)<V(B)V(A)=V(B)
NaOH溶液放置于空气中,因NaOH与空气中CO2反应造成NaOH减少,故溶液的pH减小。用H2SO4滴定Na2CO3溶液,反应分两个阶段进行:① (此时溶液呈弱碱性)② (此时溶液呈弱酸性)滴定过程中,按哪种反应进行,取决于选择的指示剂。
(1)若选用甲基橙作指示剂,因其变色范围在pH=3.1~4.4。故滴定反应按②进行,由关系式:2NaOHNa2CO3CO2↑可知消耗的H2SO4量不变,故答案为V(A)=V(B)。2H+CO2(2)若选用酚酞作指示剂,酚酞的变色范围为pH=8~10,滴定反应按①进行,由关系式:2NaOHNa2CO3NaHCO3可知消耗H2SO4的量减少,故答案为V(A)<V(B)。CO2H+
测血钙的含量时,可将2.0mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用KMnO4酸性溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20.0mL1.0×10-4mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式:______________________________________________________。(2)判断滴定终点的方法是______________________________________。(3)计算:血液中含钙离子的浓度为__________g·mL-1。2Mn2++10CO2↑+8H2O溶液由无色变为浅紫色,且半分钟内不褪色1.0×10-4
因为KMnO4溶液至反应完毕过量时,会使溶液呈紫色,故可用滴入一滴KMnO4酸性溶液由无色变为浅紫色且半分钟不褪色的方法来判断终点。由题意知可能发生反应的离子方程式为2MnO-4+5H2C2O4+6H+2Mn2++10CO2↑ +8H2O、Ca2++C2O2-4CaC2O4↓、CaC2O4+2H+Ca2++H2C2O4。
设2mL血液中含Ca2+的物质的量为x,则5Ca2+~5CaC2O4~5H2C2O4~2MnO-452x20.0×10-3L×1.0×10-4mol·L-1x=5.0×10-6mol,1mL血液中Ca2+的浓度为
1.(2010·天津)下列液体均处于25℃,有关叙述正确的是()A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
强酸的酸式盐如NaHSO4溶液的pH<7,A错误;pH=4.5的溶液中c(H+)=10-4.5mol·L-1、pH=6.5的溶液中c(H+)=10-6.5mol·L-1,B正确;同浓度CaCl2和NaCl溶液中,CaCl2溶液中的c(Cl-)是NaCl溶液中的c(Cl-)的2倍,AgCl在CaCl2溶液中溶解度小,C错误;依电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+),因为c(OH-)c(Na+),D错误。B
2.(2010•江苏)常温下,下列各组离子在指定溶液中能大量共存的是()A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+B.由水电离的c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-D.c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、SCN-
A中Fe2+、NO3-、H+会发生氧化还原反应;B项,符合条件的溶液可能是强酸性溶液也可能是强碱性溶液,HCO3-既与H+反应,又与OH-反应,B错误;c(H+)/c(OH-)=1012的溶液为强酸性溶液,离子可以大量共存;Fe3++3SCN-Fe(SCN)3,D错误。C
3.(2010·海南)常温下,将0.1mol·L-1氢氧化钠溶液与0.06mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于()A.1.7B.2.0C.12.0D.12.4假设溶液为1L,n(H+)=0.12mol、n(OH-)=0.1mol,酸过量。反应后溶液中c(H+)=(0.12mol-0.1mol)/2L=0.01mol·L-1,pH=2.0。B
4.(2010·重庆)pH=12的两种一元酸x和y,体积均为100mL,稀释过程中pH与溶液体积的关系如下图所示。分别滴加NaOH溶液(c=0.1mol·L-1)至pH=7,消耗NaOH溶液的体积为Vx、Vy,则()A.x为弱酸,VxVyC.y为弱酸,VxVy
一元酸x和y均由100mL稀释至1000mL时,酸x的pH由2变为3,酸y的pH由2变为2.5,则x是强酸,y是弱酸,酸y的浓度大。分别滴加NaOH溶液(c=0.1mol·L-1)至pH=7,弱酸消耗NaOH溶液体积大,即VxbB.在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7C.1.0×10-3mol·L-1盐酸的pH=3.0,1.0×10-8mol·L-1盐酸的pH=8.0D.若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11
酸稀释c(H+)减小,pH增大,A错误;酚酞的变色范围为8~10,溶液恰好无色时,pH可能大于7,B错误;酸的pH一定不能大于7,C错误;酸碱混合后,pH=7,所以c(H+)·V(HCl)=c(OH-)·V(NaOH),10-1×1=c(OH-)×100,所以c(OH-)=10-3mol·L-1,D正确。D
4、教学必须从学习者已有的经验开始。——杜威5、构成我们学习最大障碍的是已知的东西,而不是未知的东西。——贝尔纳6、学习要注意到细处,不是粗枝大叶的,这样可以逐步学习摸索,找到客观规律。——徐特立7、学习文学而懒于记诵是不成的,特别是诗。一个高中文科的学生,与其囫囵吞枣或走马观花地读十部诗集,不如仔仔细细地背诵三百首诗。——朱自清8、一般青年的任务,尤其是共产主义青年团及其他一切组织的任务,可以用一句话来表示,就是要学习。——列宁9、学习和研究好比爬梯子,要一步一步地往上爬,企图一脚跨上四五步,平地登天,那就必须会摔跤了。——华罗庚10、儿童的心灵是敏感的,它是为着接受一切好的东西而敞开的。如果教师诱导儿童学习好榜样,鼓励仿效一切好的行为,那末,儿童身上的所有缺点就会没有痛苦和创伤地不觉得难受地逐渐消失。——苏霍姆林斯基11、学会学习的人,是非常幸福的人。——米南德12、你们要学习思考,然后再来写作。——布瓦罗14、许多年轻人在学习音乐时学会了爱。——莱杰15、学习是劳动,是充满思想的劳动。——乌申斯基16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东18、只要愿意学习,就一定能够学会。——列宁19、如果学生在学校里学习的结果是使自己什么也不会创造,那他的一生永远是模仿和抄袭。——列夫·托尔斯泰20、对所学知识内容的兴趣可能成为学习动机。——赞科夫21、游手好闲地学习,并不比学习游手好闲好。——约翰·贝勒斯22、读史使人明智,读诗使人灵秀,数学使人周密,自然哲学使人精邃,伦理学使人庄重,逻辑学使人善辩。——培根23、我们在我们的劳动过程中学习思考,劳动的结果,我们认识了世界的奥妙,于是我们就真正来改变生活了。——高尔基24、我们要振作精神,下苦功学习。下苦功,三个字,一个叫下,一个叫苦,一个叫功,一定要振作精神,下苦功。——毛泽东25、我学习了一生,现在我还在学习,而将来,只要我还有精力,我还要学习下去。——别林斯基13、在寻求真理的长河中,唯有学习,不断地学习,勤奋地学习,有创造性地学习,才能越重山跨峻岭。——华罗庚52、若不给自己设限,则人生中就没有限制你发挥的藩篱。53、希望是厄运的忠实的姐妹。54、辛勤的蜜蜂永没有时间悲哀。55、领导的速度决定团队的效率。56、成功与不成功之间有时距离很短只要后者再向前几步。57、任何的限制,都是从自己的内心开始的。58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。59、不要说你不会做!你是个人你就会做!60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。64、每一个发奋努力的背后,必有加倍的赏赐。65、再冷的石头,坐上三年也会暖。66、淡了,散了,累了,原来的那个你呢?67、我们的目的是什么?是胜利!不惜一切代价争取胜利!68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。70、平凡的脚步也可以走完伟大的行程。71、胜利,是属于最坚韧的人。72、因害怕失败而不敢放手一搏,永远不会成功。73、只要路是对的,就不怕路远。74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。3、上帝助自助者。24、凡事要三思,但比三思更重要的是三思而行。25、如果你希望成功,以恒心为良友,以经验为参谋,以小心为兄弟,以希望为哨兵。26、没有退路的时候,正是潜力发挥最大的时候。27、没有糟糕的事情,只有糟糕的心情。28、不为外撼,不以物移,而后可以任天下之大事。29、打开你的手机,收到我的祝福,忘掉所有烦恼,你会幸福每秒,对着镜子笑笑,从此开心到老,想想明天美好,相信自己最好。30、不屈不挠的奋斗是取得胜利的唯一道路。31、生活中若没有朋友,就像生活中没有阳光一样。32、任何业绩的质变,都来自于量变的积累。33、空想会想出很多绝妙的主意,但却办不成任何事情。34、不大可能的事也许今天实现,根本不可能的事也许明天会实现。35、再长的路,一步步也能走完,再短的路,不迈开双脚也无法到达。'
您可能关注的文档
- 北师大一年级上册数学背土豆7的加减法教学课件PPT模板下载.pptx
- 七年级美术第二单元 第二课_在校园中健康成长教学课件PPT.ppt
- 徐志摩《再别康桥》精选课件PPT.ppt
- 鸦片战争课件PPT.ppt
- 《将心比心》课件PPT.ppt
- 落花生管延勋课件PPT课件.ppt
- 知识拓展课程选修课程的开发课件PPT课件.ppt
- 电工补课课件PPT课件.ppt
- 波谱分析辅导课件PPT课件.ppt
- 水溶液中的离子平衡1(33份打包) 4(课件PPT).ppt
- 水溶液中的离子平衡2(14份打包)(课件PPT).ppt
- 水溶液中的离子平衡1(33份打包) 3(课件PPT).ppt
- 水溶液中的离子平衡2(14份打包) 4(课件PPT).ppt
- 水溶液中的离子平衡2(14份打包) 2(课件PPT).ppt
- 水溶液中的离子平衡2(14份打包) 3(课件PPT).ppt
- 氯气的性质5(课件PPT).ppt
- 氨硝酸硫酸2(课件PPT).ppt
- 氨与铵态氮肥 2(课件PPT).ppt