- 1.55 MB
- 2022-04-29 14:44:02 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'第6章-醇酚醚
本章主要内容第一节醇一、结构、分类、命名法二、性质(一)物理性质(二)化学性质三、常见的醇第二节酚一、结构、分类和命名法二、性质(一)物理性质(二)化学性质三、常见的酚第三节醚一、结构、分类和命名二、性质(一)物理性质(二)化学性质三、常见的醚
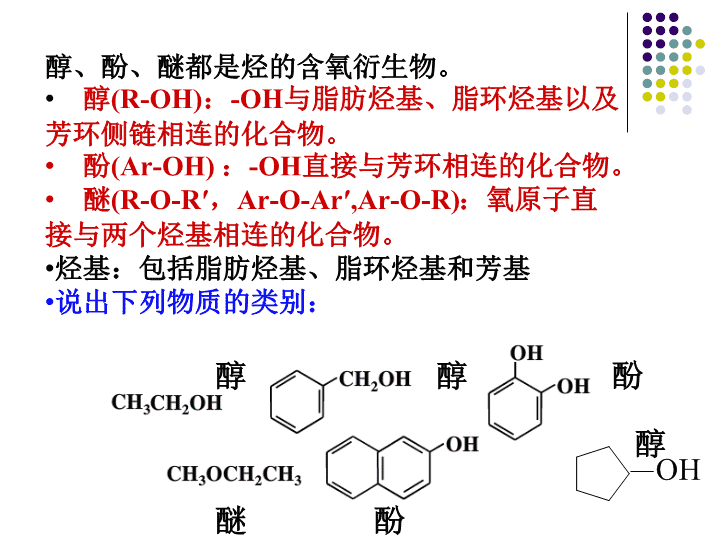
醇、酚、醚都是烃的含氧衍生物。醇(R-OH):-OH与脂肪烃基、脂环烃基以及芳环侧链相连的化合物。酚(Ar-OH):-OH直接与芳环相连的化合物。醚(R-O-R′,Ar-O-Ar′,Ar-O-R):氧原子直接与两个烃基相连的化合物。烃基:包括脂肪烃基、脂环烃基和芳基说出下列物质的类别:醇醇酚醚酚醇
3、按羟基的数目分类一元醇二元醇多元醇甲醇乙二醇丙三醇
一、结构、分类、命名法(二)命名:1.普通命名法根据烃基的名称称为“某醇”。CH3-CH2-CH2OH正丙醇CH3-CH-CH3OHCH2=CH-CH2-OH异丙醇、仲丙醇烯丙醇CH3-CH2-CH2-CH2OH正丁醇
一、结构、分类、命名法2.系统命名法(1)饱和醇选择含有-OH所连碳原子在内的最长碳链作为主链,按照主链中所含碳原子数称为“某醇”;从靠近羟基的一端开始编号,使羟基和取代基的位次尽可能小;取代基的位次、数目、名称及羟基的位次写在“某醇”之前。CH3-CH-CH-CH-CH2-CH3CH3ClOH5-甲基-4-氯-3-己醇CH3-CH-C-CH-CH2-CH3CH3OHCH3CH2CH32,4-二甲基-3-乙基-3-己醇
一、结构、分类、命名法2.系统命名法(2)不饱和醇选择含有羟基和不饱和键(双键或叁键)在内的最长碳链为主链,根据主链上所含碳原子的数目称为“某烯醇或某炔醇”。从靠近羟基一端开始编号,注明不饱和键和羟基的位次,命名为“m-某烯(炔)-n-醇”。3-丁烯-2-醇CHC-CH2OH2-丙炔-1-醇
一、结构、分类、命名法2.系统命名法(3)芳香醇可将芳基作为取代基加以命名。2-乙基-3-苯基-1-丁醇CH2CH=CH-CH2OH4-苯基-2-丁烯-1-醇
一、结构、分类、命名法2.系统命名法(4)脂环醇在环烃基的名称后加“醇”字,再从连接羟基的碳原子开始,给环上的碳原子编号,并尽量使环上取代基的位次最小。环己醇2-甲基环己醇
一、结构、分类、命名法2.系统命名法(5)多元醇选择含有尽可能多的羟基的最长碳链作为主链,根据主链上碳原子的数目和羟基的数目(用汉字)命名为“某某醇”,羟基的位次写在“某某醇”的前面。当羟基数目与主链的碳原子数目相同时,可不标明羟基的位次。丙三醇乙二醇CHCH2CH2OHOHOHOHCH2-CH2OH2,5-庚二醇
4-甲基-3-戊烯-2-醇CH2=CHCHCH2OHCH32-甲基-3-丁烯-1-醇练习:命名3-甲基-4-庚醇
1-乙基环戊醇练习:命名3-苯基-1-丙醇
二、性质(一)物理性质1.状态气味:C1—C4醇有酒味的无色液体;C5—C11的醇具有不愉快气味的油状液体;C12以上的醇为无臭无味的蜡状固体。
2.沸点氢键低级醇的沸点比相近分子量的烷烃要高得多。因为醇羟基可形成分子间氢键。
3.水溶性低级醇与水任意混溶。因为水分子与醇分子之间也能形成分子间氢键。氢键
氧化反应取代反应脱水反应酸性(被金属取代)(二)化学性质1、O-H断裂与活泼金属的反应2、C-O断裂发生取代反应和酯化反应3、脱β-H发生消除反应(脱水反应)4、脱ɑ-H发生氧化反应βɑ
1.与活泼金属反应——酸性(H被取代)H-O-H+NaNaOH+H2R-O-H+NaRONa+H2(反应激烈)(反应缓和)酸性:H2O>ROH;碱性:NaOH仲醇>伯醇叔醇容易发生分子内脱水,伯醇容易发生分子间脱水。√
(二)化学性质2)分子间脱水(取代反应)分子间脱水生成醚。CH3CH2OH+HOCH2CH3CH3CH2OCH2CH3+H2OH2SO4140℃较高温度,有利于发生分子内脱水反应;较低温度,有利于发生分子间脱水反应。
4.氧化反应a.加氧氧化氧化剂:高锰酸钾或重铬酸钾反应规律:脱-OH上的H和α-H。伯醇→醛→酸,仲醇→酮,叔醇不被氧化.+O或–H——氧化反应–O或+H——还原反应有机化合物酮醛酸√√
完成下列反应:
(二)化学性质伯醇、仲醇被氧化,而橙红色的K2Cr2O7被还原为绿色的三价铬离子。叔醇不发生反应,利用K2Cr2O7和稀硫酸溶液作氧化剂鉴别伯、仲与叔醇。酒精分析仪RCH2OHR2CHOHR3COHK2Cr2O7橙红色RCHO[O]R2C=O-RCOOH+Cr3++Cr3+(绿色)(绿色)(颜色不变)
(二)化学性质b.脱氢氧化条件:高温下和铜(或银、镍等)催化剂反应规律:脱-OH上的H和α-H。伯醇→醛,仲醇→酮,叔醇没有ɑ-H,不发生反应Cu325℃Cu325℃√√
(二)化学性质5.邻二醇的特性邻二醇:两个-OH连在两个相邻碳原子上的多元醇与新制的Cu(OH)2反应,生成深蓝色物质作用:可以鉴别具有邻二醇结构的化合物。深蓝色可溶性配合物CH2OH+CH2OHCu(OH)2CH2OCH2OCu+H2O
用化学方法区分下列各组化合物(1)正丁醇、仲丁醇和叔丁醇(2)1,3-丁二醇和2,3-丁二醇(1)加卢卡斯试剂,立即产生浑浊的是叔丁醇,放置片刻产生浑浊的是仲丁醇,数小时也不产生浑浊的是正丁醇。(2)加新制氢氧化铜,产生深蓝色的是2,3-丁二醇。练习
三、常见的醇1.甲醇甲醇又称木醇或木精,为无色透明液体具有类似酒精的气味,沸点65℃,能与水、乙醇、乙醚等混溶。甲醇具有麻醉作用,且毒性很强。饮用少量会失明,量多会致死。假酒中含有甲醇。2.乙醇俗称酒精,是饮用酒的主要成分。具有酒味的无色透明液体,沸点78.5℃,相对密度0.789g/cm3,可与水混溶。临床上用体积分数为75%的乙醇溶液做外用消毒剂,又称消毒酒精;利用乙醇挥发时能吸收热量的性质,用体积分数为25%-50%的乙醇溶液给高热患者擦浴,可以达到退热、降温的目的;体积分数为95%的乙醇又称为药用酒精,在医药中主要用于提取中草药的有效成分,配制液体试剂等。
三、常见的醇3.丙三醇丙三醇俗称甘油,为无色有甜味的粘稠液体,甘油有润肤作用,由于有吸湿性,对皮肤有刺激性,故使用时需用1:3的水稀释。临床上用甘油栓或50%甘油溶液灌肠,治疗便秘。4.戊五醇又称木糖醇,广泛存在于植物中,是多元醇中最甜的甜味剂,甜度相当于蔗糖,常用做蔗糖和葡萄糖的替代品,如用在口香糖和糖果中作为主要甜味剂。5.硫醇低级硫醇有难闻的气味,在燃气中起到报警的作用。
第二节酚一、分类、命名和结构二、性质(一)物理性质(二)化学性质1.弱酸性2.酚醚的形成3.酚酯的形成4.苯环上的取代反应5.与三氯化铁的显色反应6.氧化反应三、常见的酚
(二)酚的分类(了解)1、按酚羟基所连芳基的不同分:苯酚β-萘酚酚:羟基(-OH)直接与芳环相连的化合物。通式:Ar-OH一、分类、命名和结构(一)酚的结构
2、按酚羟基的数目分:一元酚:二元酚:多元酚:
(三)酚的命名一元酚的命名:以酚为母体,芳环上其他原子、原子团或烃基作为取代基,从连有-OH的碳原子开始编号,使取代基的代数之和最小。也可用邻、间、对表示取代基与酚羟基间的位置。苯酚OHOHCl邻氯苯酚2-氯苯酚邻甲苯酚2-甲酚OHCH3
(三)酚的命名二元酚的命名:以二酚为母体,两个酚羟基间的相对位置用阿拉伯数字或邻、间、对表示。对苯二酚1,4-苯二酚OHOH邻苯二酚1,2-苯二酚间苯二酚1,3-苯二酚
(三)酚的命名三元酚的命名:以三酚为母体,酚羟基的相对位置用阿拉伯数字或连、偏、均表示。均苯三酚1,3,5-苯三酚连苯三酚1,2,3-苯三酚偏苯三酚1,2,4-苯二酚
p-共轭C-O键牢固O-H键易于离解,即酚酸性比醇强C-O键不易断裂,酚羟基不易被取代O-H削弱苯环上电子云密度增大苯环上亲电取代反应变易,即-OH是邻对位定位基O—H二、酚的性质
二、酚的性质1.弱酸性苯酚具有弱酸性,能溶于氢氧化钠水溶液,生成可溶于水的酚钠。酸性:苯酚>水。OH+NaOHONa+H2O√强酸制弱酸强酸弱酸
二、酚的性质如果在苯酚钠溶液中加入二氧化碳,可使苯酚析出,而使溶液变浑浊;酸性:碳酸>苯酚。酸性比较:碳酸>苯酚>水>醇ONa+CO2+H2OOH+NaHCO3强酸弱酸强酸制弱酸
2.与三氯化铁的显色反应不同的酚所产生的颜色不相同,可用于酚的鉴别:OHOHOHOHOHOHOHOHOHOH紫色红棕色蓝色蓝紫色深绿色大多数酚或具有结构的脂肪族化合物与三氯化铁的水溶液作用,生成有色物质。6ArOH+FeCl3H3[Fe(OAr)6]+3HCl紫色络合物
(二)化学性质3.氧化反应(了解)酚类化合物很容易氧化,产物随氧化剂和反应条件而不同.苯酚长期与空气接触,随氧化反应的进行,颜色逐渐变深;苯酚与重铬酸钾的硫酸溶液作用,则氧化生成对苯醌(黄色晶体).OHK2Cr2O7H2SO4OO+H2O
(二)化学性质4.苯环上的取代反应酚羟基是邻、对位定位基,能使苯环活化a.卤代酚很容易进行卤化反应。苯酚与溴水在常温下即可作用,生成三溴苯酚的白色沉淀。这一反应很灵敏,可用于苯酚的鉴别。OHBr2OHBrOHBr++CS2或CCl40~5℃OH3Br23HBr++H2OOHBrBrBr-(白)√
(二)化学性质b.硝化苯酚在室温下与稀硝酸作用生成邻硝基苯酚和对硝基苯酚的混合物,混合物可用水蒸气蒸馏法分离.OH稀HNO3OHNO2OHNO2++20℃
对硝基苯酚可以在分子间形成氢键。邻硝基苯酚可以在分子内形成氢键。OHNO2OHNO2OHNO2沸点℃:100194279ONH=OOHONO=OHONO=O分子内氢键,沸点较低。分子间氢键,沸点较高。
(四)苯环上的取代反应c.磺化在25℃时,主要产物为邻羟基苯磺酸;在100℃时,主要产物为对羟基苯磺酸。OHOH浓H2SO4OH2SO3H25℃SO3H100℃
三、常见的酚1.苯酚俗称石炭酸,因最初是从煤炭中提取的,又具有弱酸性而得名。具有特殊气味,常被空气氧化变为粉红色,常温下微溶于水而使溶液呈现浑浊。苯酚具有杀菌作用,常用作消毒剂和防腐剂,但有毒及腐蚀性,使用时要小心。2.甲酚因其来源于煤焦油,又名煤酚,有3种异构体,分别是邻甲酚、间甲酚、对甲酚。有杀菌能力,能溶于肥皂溶液,常配制成50%的肥皂溶液,称为煤酚皂液,俗称“来苏儿”,用于器械和环境消毒。
第三节醚一、结构、分类和命名二、性质(一)物理性质(二)化学性质1.盐的生成2.醚键的断裂反应3.过氧化物的生成三、重要的醚
一、结构、分类和命名(一)结构醚:氧原子直接与两个烃基相连的化合物,可以看成水分子中的两个氢原子被烃基取代生成的化合物。通式:R-O-R’、Ar-O-Ar’、R-O-Ar官能团:醚分子中含有两个碳氧单键,称为醚键。例如:甲醚CH3OCH3
R=R’?按烃基分R=R’:R≠R’:单醚混醚饱和醚不饱和醚芳香醚(含有芳香烃基)环醚(二)分类单醚:与氧相连的两个烃基相同。混醚:与氧相连的两个烃基不同。
(三)命名1.单醚在醚字前面加上烃基的名称,称“某醚”。CH3-O-CH3甲醚C2H5OC2H5乙醚CH2=CH-O-CH=CH2乙烯醚
2.混醚脂肪混醚:按小的烃基在前,大的烃基在后,命名为“某某醚;芳香混醚:按芳基在前,烷基在后,命名为“某某醚。CH3-O-C(CH3)3甲基叔丁基醚乙基乙烯基醚苯甲醚CH2=CH-O-CH2CH3甲乙醚
3.环醚环醚:碳氧形成三元环的化合物,叫做“环氧某烷”。环氧乙烷CH2OCH2OCH2CH3CH21,2-环氧丙烷2,3-环氧丁烷
4.复杂醚用系统命名法:将较小的烷氧基(-OR)作为取代基,较大的烃基作母体来命名。1234563-乙氧基已烷3-甲氧基-1-丙烯(甲基烯丙基醚)123
二、性质(一)物理性质在常温下除甲醚和甲乙醚为气体外,大多数醚为易燃的液体,有特殊气味,相对密度小于1。低级醚的沸点比相对分子质量相近的醇的沸点低得多。醚一般微溶于水,易溶于有机溶剂。由于醚在许多反应中活性很低,所以在有机反应中常用醚作溶剂,常用来提取有机物或作有机反应的溶剂。(二)化学性质醚键(C-O-C)是醚的官能团,比较稳定,所以醚对碱、氧化剂、还原剂都很稳定;在常温下醚也不与金属钠作用。但是在一定条件下,醚也能发生某些化学反应。
(二)化学性质醚分子的氧原子有未共用电子对,能接受质子,所以醚能与强酸作用,以配位键的形式结合生成佯盐。佯盐很不稳定,在水中立即分解,又重新分出醚。利用此性质可将醚从烷烃或卤代烃中分离出来。1.佯盐的生成(了解)
(二)化学性质2.醚键的断裂反应醚与强无机酸(浓HI)作用,醚键断裂.反应规律:O归大烃基所有,O与H结合。含有两个不同烷基的混合醚,与氢碘酸作用时,一般是较小的烷基形成碘代烷。HICH3OCH2CH2CH3CH3I+HOCH2CH2CH3
(二)化学性质2.醚键的断裂反应反应规律:O归大烃基所有,O与H结合。芳基烷基醚与氢碘酸作用时,总是烷氧键断裂,生成酚和碘代烷。OC2H5OHC2H5I△HI+
(二)化学性质3.过氧化物的生成醚对氧化剂较稳定,但长期与空气接触可被空气中的氧氧化为有机过氧化物。醚的过氧化物不稳定,在加热或蒸馏的过程中很容易分解而发生猛烈的爆炸,所以蒸馏醚类化合物时,一般不宜蒸干。久置的醚在使用前,应先检测是否含有过氧化物。过氧化物OOHO2CH3CH2-O-CH2CH3CH3CH2-O-CHCH3
(二)化学性质检验过氧化物的方法:A.可用硫酸亚铁和硫氰化钾溶液,溶液变红,证明有过氧化物存在。B.可用碘化钾-淀粉试纸检验,试纸变蓝,证明有过氧化物存在。CNS-红色+过氧化物++-¾®¾®3632)(FeFeSCNFe淀粉蓝色过氧化物¾®®+2II-可用硫酸亚铁水溶液或亚硫酸钠溶液等还原剂洗涤醚,可破坏其中的过氧化物。
课堂思考题1.下列化合物哪些能与FeCl3溶液发生颜色反应?()A:甲苯B:苯酚C:2,4-戊二酮D:苯乙烯2.苯酚可以用下列哪种方法来检验?()A:加漂白粉溶液B:加Br2水溶液C:加酒石酸溶液D:加CuSO4溶液3.下列化合物能形成分子内氢键的是?()A:对硝基苯酚B:邻硝基苯酚C:邻甲苯酚D:苯酚BBB
作业P79目标检测一、二(做书上)三、四、五(上交)六(思考)
阴阳与健康陈翔宇、文山、许可、周宁、汪杰、曾勇、巫亮、郑粮玮、芦苇、龙涛
《黄帝内经》:阳者,天气也,主外;阴者,地气也,主内;阴阳者,天地之道,万物之纲纪,变化之父母,生杀之本始,神明之府也,治病必求于本。一、阴阳的概念
1、人体中:上为阳,下为阴;背为阳,腹为阴;体表为阳,体内为阴。心、肝、肺、脾、肾五脏为阴,胆、胃、大肠、小肠、膀胱、三焦六腑为阳。2、具体到每一脏腑,则又有阴阳之分,即心有心阴、心阳;肾有肾阴,肾阳等。3、气血津液等物质属于阴,发挥的功能作用属于阳。
二、阴阳失衡则患病(一)、阴阳平衡的概念对人体来说,阴阳平衡包括内在平衡和外在平衡两方面。内在平衡是指脏腑、器官、组织、细胞之间相互协调一致的状态。外在平衡是指人体的阴阳要与所处环境的阴阳相互协调一致,也就是人要与自然相适应。这两个都做到了,就达到阴阳平衡了。
人体阴阳平衡,则五脏六腑功能正常,那么,人体的生理功能就能正常。表现在以下各个方面:机体的生长、发育正常,头脑清楚,思维敏捷,精神充沛,精神愉快,心情舒畅,面色红润光泽,眼睛明亮有神,视物清楚,听觉、嗅觉灵敏,声音洪亮,肌肉发达,丰满健壮,骨骼结实强壮,皮肤致密,毛发光泽,抗病能力强,消化吸收好,二便正常。
(二)、阴阳失衡致患病要想阴阳平衡,就必须要保持经络的畅通。因为经络是一条通道:它是经气运行的通道;也是联系四肢百骸,五脏六腑的通道;还是联系大自然,沟通内外环境的通道。由此可知,经络是非常重要的。只有经络保持通畅,阴阳才能平衡,人才能健康。如果经络不通,就会使阴阳二气运行受阻,则阴阳互根互用,相互化生转换的特点得不到体现,最终会导致阴阳失衡,出现各种症状。这就是所说的阴阳失衡人患病。
1.肝的阴阳失调有肝气郁结、肝火上炎、肝阳上亢、肝阴虚、肝血虚、肝阳虚、肝气虚、肝胆湿热、肝风内动等。见于肝胆疾病,乳腺疾病,甲状腺疾病,关节周围疾病,高血压,中风,目疾,月经病,腹痛疝气,外因病,某些消化系统疾病等等。阴阳失衡的表现
1.肝与胆:肝胆有病时常见以下症状:①眩晕或偏头痛、巅顶痛;②双目干涩、目赤、事物模糊;③口干苦;耳鸣、耳聋;④指甲无华或有斑点;⑤四肢拘挛抽搐、肌肉震颤、手足麻木、膝部屈伸不利;⑥胁肋、少腹胀痛;⑦急躁易怒忧郁胆怯、多梦易惊;⑧面色萎黄、脱发;⑨生殖系统疾病;⑩黄疸
2.心的阴阳失调有心气虚、心阳虚、心阴虚、心血虚、心血瘀阻、心火亢盛、痰迷心窍等等。见于冠心病、心梗、心慌、心悸、胸闷、胸痛、失眠、癫痫等等。
2.心与小肠:心、小肠有病时常见以下症状:①心悸、怔忡;②心烦、心痛;③舌尖起刺,舌体强硬,言语不利;④失眠多梦;⑤健忘;⑥神昏、谵语;⑦小便赤涩;
3.脾胃的阴阳失调有脾胃气虚、脾胃阴虚、脾胃虚寒、脾胃湿热、脾不统血等。见于消化系统疾病(如胃炎、胃溃疡、十二指肠炎等),糖尿病,内脏下垂(胃下垂、子宫下垂、脱肛等),月经病,多种出血症状,腹痛,便秘或便溏等等。
3.脾与胃:脾胃有病时常见以下症状:①纳差,不欲饮食;②脘腹胀满或疼痛;③腹泻或便溏;④便秘;⑤浮肿;⑥各种出血(便血、吐血、崩漏等等);⑦嗳气、呃逆;⑧呕吐;
4.肺的阴阳失调有肺气虚、肺阴虚、寒邪袭肺、热邪犯肺等。见于肺病及呼吸系统疾病(咳嗽、哮喘、气管炎、肺气肿等),皮肤病(皮炎、皮疹、色斑、皮癣、疣等),便秘、便溏或大便失禁等等。
4.肺与大肠:肺、大肠有病时常见以下症状:①恶寒、发热;②咳嗽;③喘;④咳痰或咯血;⑤胸闷或痛;⑥声音改变;⑦鼻塞流涕;
5.肾的阴阳失调有肾阴虚、肾阳虚、肾气虚、肾精不足等。见于腰膝酸软疼痛、早衰、肾炎、尿毒症、骨病(颈椎病、腰椎病、骨质增生、骨质疏松、强直性脊柱炎、类风湿性关节炎等)、生殖系统疾病(男子阳萎遗精,精少不育;女子月经不调,经闭不孕)、二便异常等等。
5.肾与膀胱:肾、膀胱有病时常见以下症状:①腰膝酸痛无力;②骨关节疼痛不适;③耳鸣、耳聋;④头发变白或脱发;⑤牙齿脱落;⑥男子阳萎遗精,精少不育;⑦女子月经不调,经闭不孕;⑧水肿;⑨二便异常;
四、阴阳离绝人死亡阴阳是互为存在的,他们各自都是对方存在的基础,能够互相转化。如果没有阳,自然就没有阴;没有阴,当然就谈不到阳了。就像《黄帝内经》说的“孤阴不长,孤阳不生”“无阳则阴无以化,无阴则阳无以生”。
这时可见突然面色晦暗,口唇青紫,冷汗如膏,四肢厥冷,心悸气短,呼吸微弱,神志不清等等。经络堵塞,就会阻断人体脏腑阴阳二气与外界阴阳二气进行信息能量交换的通道,就会导致阴阳离绝。代表事物的消亡,对人来说就意味着生命的完结。'
您可能关注的文档
- 最新第5章细菌的遗传与变异课件PPT.ppt
- 最新第5章遥感图像的目视解译与制图课件PPT.ppt
- 最新第5章长期投资方式课件PPT.ppt
- 最新第5讲影响药物作用因素-传出神经药理浅论幻灯片(1)课件PPT.ppt
- 最新第5讲 B型超声诊断仪扫描原理b课件PPT.ppt
- 最新第5课-画地图-讲历史---学习与探究之一课件PPT课件.ppt
- 最新第6章-动物界-脊索动物门-1课件PPT.ppt
- 最新第6章-酒店产品设计与创新(1)课件PPT.ppt
- 最新第6章-骨骼肌肉系统常见病损的康复课件PPT.ppt
- 最新第6章信号分析和频域测量.课件PPT.ppt
- 最新第6章牙周病的预防课件PPT.ppt
- 最新第6章楼梯的构造与施工素材课件PPT.ppt
- 最新第6节 葡萄膜病课件PPT.ppt
- 最新第6节-电能(第二课时)课件PPT.ppt
- 最新第7章-光栅传感器课件PPT.ppt
- 最新第7章--集装箱货物运输分解课件PPT.ppt
- 最新第7章---红外传感器课件PPT.ppt
- 最新第7章-其他常用机构课件PPT.ppt