- 587.00 KB
- 2022-04-29 14:31:48 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'时水的电离和溶液的酸碱性
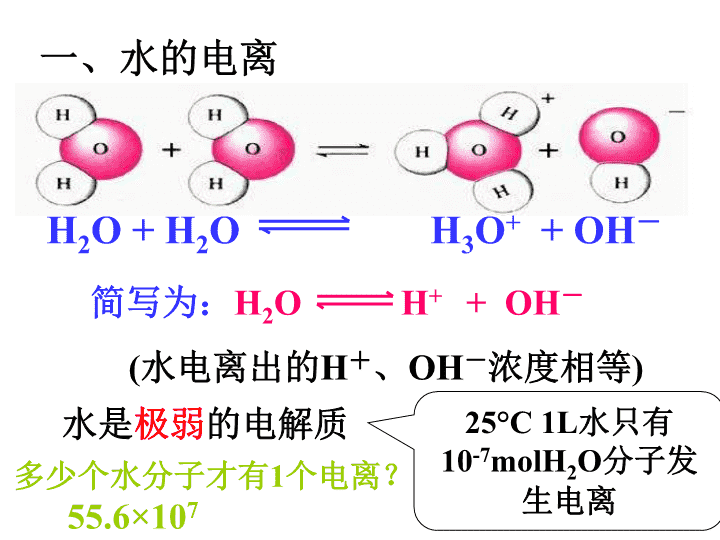
H2O+H2OH3O++OH-简写为:H2OH++OH-(水电离出的H+、OH-浓度相等)一、水的电离水是极弱的电解质25°C1L水只有10-7molH2O分子发生电离多少个水分子才有1个电离?55.6×107
K电离=c(H+)×c(OH-)c(H2O)K.=c(H+).c(OH-)c(H2O)Kw=c(H+).c(OH-)其中常数K与常数c(H2O)的积记为Kw,称为水的离子积常数,简称为离子积H2OH++OH-
水的电离水的离子积:影响因素KW=c(OH-)·c(H+)(25℃时,KW=1.0×10-14)温度:酸:碱:T↑,KW↑抑制水的电离,KW不变抑制水的电离,KW不变3、无论是酸溶液还是碱溶液中都同时存在H+和OH-!注意:1、在任何水溶液中,均存在水的电离平衡,Kw=c(H+)·c(OH-)均成立。(25℃时Kw=10-14)2、水电离出的H+、OH-永远相等H2OH++OH-
(2)、下列物质溶解于水时,电离出的阴离子能使水的电离平衡向右移动的是()A、CH3COONaB、Na2SO4C、NH4ClD、CH3COOHA(1)下列微粒中不能破坏水的电离平衡的是()A、H+B、OH-C、S2-D、Na+D【课堂练习】
(3)某温度下纯水中C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=___________。若温度不变,滴入稀盐酸使C(H+)=5×10-6mol/L,则此时溶液中的C(OH-)=___________2×10-7mol/L8×10-9mol/L(4)在常温下,0.1mol/L的盐酸溶液中水电离出的C(H+)和C(OH-)是多少?水电离出的C(OH-)=1×10-14/0.1=1×10-13mol/L=C(H+)水【课堂练习】在常温下,0.1mol/L的NaOH溶液中水电离出的C(H+)和C(OH-)是多少?
(5)在常温下,由水电离产生的C(H+)=1×10-13mol/l的溶液,则该溶液的酸碱性如何?答:可能是酸性也可能是碱性(6)某溶液中由水电离出来的C(OH-)=10-12mol/L,则该溶液中的溶质不可能是()A、HClB、NaOHC、NH4ClD、H2SO4C
课堂练习7.室温下,由水电离产生的c(OH-)=10-11mol/L的溶液中,一定大量共存的离子组()A.Na+、NH4+、Cl-、SO42-B.S2-、CH3COO-、Na+、NH4+C.K+、Na+、HCO3-、NO3-D.K+、Na+、NO3-、SO42-一定可能DAD
水的离子积常数Kw=c(H+).c(OH-)对水电离平衡的影响c(H+)mol/Lc(OH-)mol/Lc(H+)与c(OH-)比较溶液酸碱性纯水无=10-7=10-7c(H+)=c(OH-)中性HCl左移>10-7<10-7c(H+)>c(OH-)酸性NaOH左移<10-7>10-7c(H+)
您可能关注的文档
- 最新日出授课课件资料课件PPT.ppt
- 最新无锡市快速公交体系研究课件PPT.ppt
- 最新早教市场推广方式课件PPT.ppt
- 最新日食和月食简析课件PPT我制作的ppt课件.ppt
- 最新时尚经典高端共赢未来商务风工作总结汇报PPT模板课件PPT.ppt
- 最新时千米的认识2课件PPT.ppt
- 最新时鸟恋蓝天鱼恋水下课件PPT.ppt
- 最新时诚实守信课件PPT.ppt
- 最新时评类联系实际4月初资料课件PPT.ppt
- 最新时杂化轨道的判断方法总结分析课件PPT.ppt
- 最新时打扫卫生课件PPT.ppt
- 最新时异分母分数加减课件PPT.ppt
- 最新映日荷花别样红课件PPT.ppt
- 最新春季传染疾病防控教育课件PPT.ppt
- 最新春天的花课件PPT.ppt
- 最新春游前安全教育课件PPT.ppt
- 最新春季常见传染病防治普及知识讲座课件PPT.ppt
- 最新春季常见传染病及预防知识课件PPT.ppt