- 3.36 MB
- 2022-04-29 14:22:48 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'北京教育科学研究院基础教育基地教学研究中心高一化学教师培训资料课件-人教版必修1
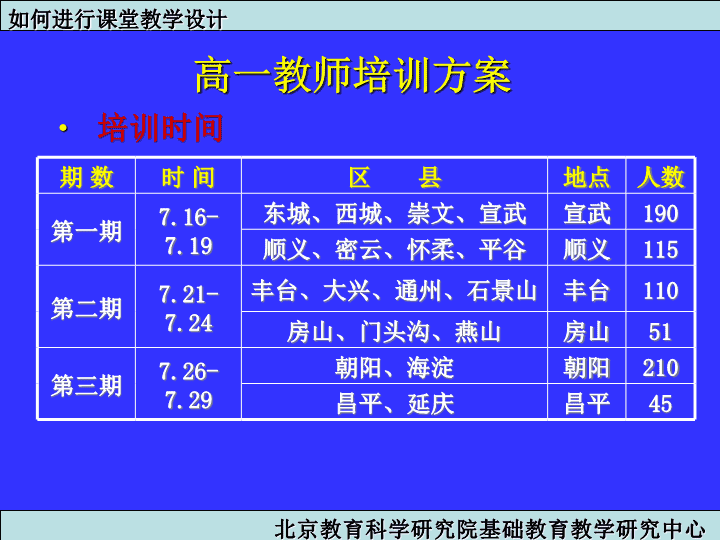
高一教师培训方案培训时间期数时间区县地点人数第一期7.16-7.19东城、西城、崇文、宣武宣武190顺义、密云、怀柔、平谷顺义115第二期7.21-7.24丰台、大兴、通州、石景山丰台110房山、门头沟、燕山房山51第三期7.26-7.29朝阳、海淀朝阳210昌平、延庆昌平45
编写目的进一步熟悉课程标准、指导意见及模块学习要求、教材,理解新课程的目标、结构及内容特点。合作编写单元(节)教学设计,选择优秀上传教师研修网重点:课时的控制、内容深广度的把握、开放性与实效性的有机结合。为教师继续撰写课时教学设计提供参考。编写单元教学设计
一、教学设计与教案的区别(二)指导思想不同教案是“课堂、教师、教材”为中心的传统教学思想的体现,它的核心目的就是教师怎样讲好教学内容。教学设计不仅重视教师的教,更重视学生的学,以及怎样使学生学得更好,达到更好的教学效果是教学设计的指导思想,所以对学生进行特征分析是教学设计不可缺少的步骤,体现了现代教学理论的鲜明性。
一、教学设计与教案的区别(三)层次不同教学设计的范围可以大到一个学科、一门课程,也可小到一节课、一个问题的解决。教学设计可分为许多层次:学科教学设计、模块教学设计、主题教学设计、单元教学设计、课堂(课时)教学设计等。课堂教学设计只是教学设计中运用最多的一个层次,而且从研究范围上讲教案只是教学设计的一个重要内容,因此教学设计与教案的层次关系是不完全对等的。
二、课堂教学设计的基本内容(一)必修课教学设计的基本思路(二)章教学设计的主要内容(三)节(单元)教学设计的主要内容
(一)必修课教学设计思路教学内容概述本章内容在模块中的地位和作用三维目标分析重难点分析教学过程设计学时建议教学方式和方法分析教学资源建议
(二)章教学设计的主要内容化学必修1第一章从实验学化学第二章化学物质及其变化第三章金属及其化合物第四章非金属及其化合物化学必修2第一章物质结构元素周期律第二章化学反应与能量第三章有机化合物第四章化学与自然资源的开发利用结合模块学习要求进行分析
(二)节教学设计的主要内容(一)学习目标分析(二)重难点分析(三)教学内容安排(四)主要教学过程设计(可以分课时写)(五)教学资源建议(六)教学方法与学习指导策略建议(七)课堂评价建议样例1样例2
(二)节教学设计的主要内容撰写要求1.以节为单位,多人合作完成,体现整体设计的思想。2.不只罗列内容,而且要有分析。3.注意问题:内容之间的相互联系;内容深广度的把握;开放性与实效性的有机结合。
主要教学过程设计(一)——化学反应的限度
关注学生的原认知水平及新认知脉络学生已经知道了什么?(先前经验)学生还想知道什么?(自发动机)学生能知道什么?(教学目标)学生如何知道什么?(教学过程)
课例分析课例:化学反应的限度思考问题:(1)学生已有的对化学反应的认识有哪些?(2)学生可能还想知道哪些有关化学反应的问题?(3)通过这一节学习,学生能获得哪些新认识?
设计方案一引入提出问题:碘极易溶于KI中,反应生成KI3,反应后溶液仍体现碘的化学性质。师生交流研讨、实验探究:碘过量碘少量反应后溶液都表现出碘的性质交流研讨得出结论得出可逆反应概念提出问题何时达到反应的最大程度?提供数据SO2与O2反应时间与各物质的浓度学生绘制图形浓度随反应时间变化的图像速率随反应时间变化的图像交流研讨得出结论反应平衡状态的特征
设计方案二
设计方案三
1.明确知识对深化、发展学生的认识的作用;2.关注知识的形成、发展过程;3.注重知识形成与发展的层次性。要认真思考通过哪些素材形成学生的核心知识,设计哪些活动使学生认识和理解有关知识问题线索知识脉络认知脉络解决问题的证据教学设计原则如何进行教学设计
1.分析教材:——知识线索(正文)——确定知识的深广度及呈现方式——活动线索(活动性栏目)——确定教学过程的学生活动——资料线索(资料性栏目或正文)——选择合适的STS内容进行教学设计的几个环节
交流与研讨:在原有认识化学反应的基础上,进行设问。阅读与研讨:有一类反应不能完全进行;体会这类反应在实际中的存在。
小结整理:得出可逆反应的概念。体会研究可逆反应的实际意义思考与交流:结合具体、实际反应,加深对可逆反应的理解读图讨论:得出化学平衡状态的特征之一是正、逆反应速率相等。研讨得出另一个主要特征:物质浓度不再改变。
建议通过实验探究得出:外界条件改变时,会改变一个化学反应的限度。(可以选择NO2在温度改变时平衡移动的实验)
教学设计思路:新课引入认识化学反应的新视角可逆反应宏观、微观两个视角化学平衡状态化学平衡状态的移动本节教学的重点和难点,包括形成概念和深化理解概念两个环节通过实验获得感性认识
1.分析教材——分析本部分内容在教材中的地位和作用;——分析本部分内容的知识脉络;——确定可用的教学素材2.分析学生——分析学生的认识脉络;——确定问题线索;——确定学生解决问题需要的证据;进行教学设计的几个环节
问题线索知识脉络认知脉络解决问题的证据化学平衡(概念、特点)化学平衡的移动可逆反应化学平衡状态的特点可逆反应的特点(能同时向正、逆两个方向进行)可逆反应“结束”时即达化学平衡状态有些化学反应不能将反应物完全转化成产物化学平衡状态的移动
与不可逆反应比较,可逆反应有什么特点?(宏观)为什么可逆反应中,反应物不能被全部消耗?可逆反应真的停止了吗?如何解释?可逆反应是否会“停止”?如何判断?化学平衡状态概念的建立及深化理解条件改变时,化学平衡状态会改变吗?数据微观图示数据教师讲述实验探究具体的化学反应
1.分析教材——分析本部分内容在教材中的地位和作用;——分析本部分内容的知识脉络;——确定可用的教学素材2.分析学生——分析学生的认识脉络;——确定问题线索;——确定学生解决问题需要的证据;进行概念教学的教学设计的几个环节3.完成教案4.进行课后反思
案例展示:化学反应的限度
观察下列各组化学方程式,寻找每组内两个化学反应的异同,谈谈你对化学反应的认识。(1)2H2+O2===2H2O(放热反应)2H2O===2H2+O2(吸热反应)点燃通电(2)Fe+2HCl(浓)==FeCl2+H2↑Fe+2HCl(稀)==FeCl2+H2↑(3)2CO+O2===2CO22SO2+O22SO3点燃△催化剂可逆反应提出问题1:可逆反应有什么特点?新课引入
观察下列数据,思考:与不可逆反应比较,可逆反应有什么特点?通过表中数据,你能发现什么?表1:反应中,0.040.10.140.21.2反应结束后SO2物质的量10010510.5n(O2)/mol22222n(SO2)/mol2SO2+O22SO3△催化剂表2:反应中,00001反应结束后CO物质的量10010510.5n(O2)/mol22222n(CO)/mol2CO+O2===2CO2点燃认识可逆反应
观察上图,用你的语言描述上图所表示的反应的进行情况,思考:为什么可逆反应中,SO2等反应物不可能被全部消耗?图中:表示SO2分子;表示O2分子;表示SO3分子认识可逆反应问题2
(小结、板书)1.什么是可逆反应?2.可逆反应的特点3.正反应、逆反应提出问题3:可逆反应会“停止”吗?
观察下列数据表,思考:反应进行到什么时候“停止”了?说明你的理由。2SO2+O22SO3△催化剂时间(min)物质的量浓度(mol/L)010203040506070SO210753.52111O253.52.51.7510.50.50.5SO30356.58999建立化学平衡提出问题4:反应真的停止了吗?(设问)
建立化学平衡教师讲解提出问题5:化学平衡状态有什么特征?
时间(min)物质的量浓度(mol/L)010203040506070SO210753.52111O253.52.51.7510.50.50.5SO30356.58999逆反应正反应建立化学平衡
(小结、板书)化学平衡状态的特征(阅读教材)
请你根据表中数据分析,SO2与O2反应时,从反应开始至达到化学平衡状态的过程中,正、逆反应速率将如何变化?并尝试在坐标图中进行表示。vtV正V逆2SO2+O22SO3△催化剂时间(min)物质的量浓度(mol/L)010203040506070SO210753.52111O253.52.51.7510.50.50.5SO30356.58999
分小组讨论:请分析反应或N2+3H22NH3高温、高压催化剂2NO2N2O4(1)请你描述上述反应处于化学平衡状态时,在同一瞬间参加反应的各微粒间的数量关系。(2)请你在坐标图中表示出上述反应在达到化学平衡状态的过程中,正、逆反应速率的变化情况。并解释为什么在化学平衡状态时,正、逆反应依然在进行,而参加反应的各物质的浓度不变?(红棕色)(无色)vt巩固化学平衡概念提出问题6:反应条件的改变,会影响化学平衡状态吗?
实验:温度改变时,反应的化学平衡状态会改变吗?2NO2N2O4常温热水冷水实验方法:(红棕色)(无色)化学平衡的移动
讨论:1.化学平衡状态改变时,哪些物理量会发生改变?哪个物理量的变化利于观察?2.实验过程中,什么现象可以表征各物质的浓度是否发生了变化?小结:问题变量现象温度改变时,化学平衡状态是否会改变浓度是否改变颜色的变化
冷水常温热水在这张图片中,你看到了什么?你知道了什么?你得到了什么结论?
化学平衡状态怎样定量描述化学平衡状态?反应条件改变时,化学平衡将怎样移动?怎样根据化学反应的快慢和限度选择合适的反应条件?课堂总结
主要教学过程设计(二)——氨和铵盐
主要教学过程设计(一)——化学反应的限度
编写节教学设计的分工安排章节主要承担区县主要负责人化学1第一章(2节)平谷(13人)胥晓华第二章(3节)顺义(43人)李向红第三章(3节)化学2第一章(3节)怀柔(20人)崔建福第三章(4节)密云(21人)任连俊第四章(2节)平谷(13人)胥晓华
11—20各数的认识仔细看书68页、69页,72页、73页,想一想在这个单元你学会了哪些知识?青岛版一年级数学上册课件
11—20各数的认识信息窗一信息窗二数数写数数的组成计数单位数位十几加几(不进位)十几减几(不退位)加减法各部分的名称
1013141819111215161720
1215
1个十和2个一组成()。1212里面有()个十和()个一。12
10个一1个十。就是计数单位“十”
从右边起第一位是()位,第二位是()位。个十
12+3=17-4=1513加数加数和被减数减数差说一说,你是怎么算出来的?
第一关“11”这个数中的两个1意思一样吗?为什么?说一说
1个十1个一1个十和1个一合起来是11。11
第二关
(2)个十和个一组成17。(4)13前面一个数是,后面一个数是。112猜一猜(1)15里面有个十和个一。157(3)两个十是。2014
第三关
抢答题:(1)10个一是1个(),20里面有()个十。(2)7个一和1个十组成()。(3)14+3=17一个加数是(),另一个加数是(),和是()。(4)15-5=10被减数是(),减数是(),差是()。十2171731410515'
您可能关注的文档
- 最新化学能与电能(动画)概要课件PPT.ppt
- 最新化学电源ppt课件PPT.ppt
- 最新化工原理-19对流传热机理和对流传热系数..课件PPT.ppt
- 最新化工仪表及其自动化(精)课件PPT.ppt
- 最新化学键的振动频率课件PPT.ppt
- 最新化学键与物质类别ppt课件PPT课件.ppt
- 最新化工设计概论与化工制图课件--第六章-设备的选型及其工艺设计课件PPT.ppt
- 最新北京---明十三陵模板课件PPT.ppt
- 最新北京大学电分析课件电极电解质溶液界面上的双电层课件PPT.ppt
- 最新北师大图书馆学基础chapter1课件PPT.ppt
- 最新北宋建立及其制度创设(精)课件PPT.ppt
- 最新北师大版二年级数学下册《回收废电池》课件PPT版课件ppt.ppt
- 最新北师大必修一unit3-lesson4-christmas课件PPT.ppt
- 最新北师大版四年级数学下册期中复习课件课件PPT.ppt
- 最新北师大版四年级上册数学第三单元复习课件PPT课件.ppt
- 最新北师大版八年级数学下--等腰三角形(4).课件PPT.ppt
- 最新北师大版八年级下册6.1平行四边形的性质(2)课件课件PPT.ppt
- 最新北师大版五年级语文上册《生死攸关的烛光》精品课件PPT课件.ppt